Основная причина смерти населения из-за сердечно-сосудистых заболеваний [3, 6, 12]. Госпитальная летальность при остром инфаркте миокарда (ИМ) колеблется от 18,5% до 50%, в среднем составляя 30–35% у пациентов 60 лет и старше [1, 5].
Исследование INTERHEART выявило модифицированные факторы риска, на долю которых приходится более 90% риска развития острого инфаркта миокарда. В гериатрической практике наличие оценка модифицированных и немодифицированных факторов риска у пожилых пациентов проводиться по общей схеме [17], сочетанная патология больных пожилого возраста с острым коронарным синдромом с подъемом сегмента ST (ОКСпST) создает новую клиническую ситуацию, требующую учета ее особенностей при проведении тромболизиса [18], что, несомненно, отражается на исходах заболевания.
Цель исследования. Оценить влияние факторов риска на исход заболевания у больных ОКСпST пожилого и старческого возраста пуролазой в дозе 6-8 млн. МЕ и стрептокиназой 1,5 млн. МЕ.
Материалы и методы. Ретроспективный анализ историй болезни пациентов с ОКСпST в возрасте 60 - 85 лет за 2006 – 2008 г. г., которые в экстренном порядке доставлены бригадами скорой помощи в Тольяттинскую городскую больницу №2 им. В.В. Баныкина, в палату интенсивной терапии кардиологических отделений №1 и №2 для проведения тромболитической терапии (ТЛТ) пуролазой в дозе 6 млн. МЕ и 8 млн. МЕ и стрептокиназой 1,5 млн. МЕ. Всего в исследовании участвовало 278 пациентов.
Критерии включения:
- больные с ОКСпST, давностью ангинозных болей до 6 часов, при рецидиве ишемии до 12 часов; диагностика – рекомендации Всероссийского научного общества кардиологов (ВНОК) 2009 г. [2];
- возраст 60 – 85 лет;
Критерии исключения: общепринятые абсолютные противопоказания проведения ТЛТ.
Тромболизис проводился по стандартным схемам, и в дальнейшем лечение больных основывалось на рекомендациях ВНОК от 2009 г. [2]: инфузия нитроглицерина в первые сутки болезни, антиагреганты, антитромбоцитарная и антикоагулянтная терапия, бета-блокаторы, ингибиторы АПФ, статины. Ферментативная диагностика: тропонины I, МB-фракции креатинфосфокиназы (МB-КФК).
Пациенты были разделены на две группы, в зависимости от дозы получаемого тромболитика – пуролаза 6 млн. МЕ и 8 млн. МЕ – I группа и стрептокиназа 1,5 млн. МЕ – II группа. Статистический анализ проведен с использованием программы «Statistica 6,0». Количественные данные представлены в виде среднего и стандартной ошибки среднего (M ± m), обработка результатов методами непараметрической статистики, применялись критерии Вилкоксона и Манна-Уитни. Статистически значимыми считали различия при р ≤ 0,05.
Полученные результаты и обсуждение. В группах I и II включено 145 и 133 пациентов, из них мужчин – 81 (55,9%) и 84 (63%), женщины – 64 (44,1%) и 49 (37%) соответственно, р = 0,2. Вo II группе отмечался более старший возраст, чем в I – 69,8 ± 0,5 и 69,6 ± 0,5 соответственно, р = 0,1. Причем, эта тенденция наблюдается и у мужчин и у женщин.
Данные анамнеза. У всех больных отмечено две и более сопутствующей патологии. У больных в группах I и II – ишемическая болезнь сердца (ИБС), перенесенный инфаркт миокарда – 34 (23,4%) и 42 (31,6%), хроническая сердечная недостаточность (ХСН) IIА – 121 (83,4%) и 117 (88%), IIБ – 24 (16,6%) и 16 (12%) по New York Heart Association (NYHA), дисциркуляторная энцефалопатия смешанного генеза I и II – 95 (65,5%) и 89 (66,9%), пороки сердца – 19 (13,1%) и 22 (16,5%), межгрупповые различия были статистически незначимы.
Пациенты с повторными инфарктами были старше по возрасту, чем впервые поступившие с острым инфарктом миокарда (ОИМ), статистически значимые различия у мужчин в группе I (р = 0,02) и II (р = 0,05), больные в группе I с ХСН IIБ старше ХСН IIА р = 0,02. В группе I больше было больных с ожирением, чем в II – 24 (16,5%) и 12 (9,0%) соответственно, р = 0,049, женщин чаще страдали ожирением, чем мужчины и в I (р = 0,006) и во II (р = 0,009). Дислипидемии больше вo II, чем в I – 30 (23,0%) и 21 (14,4%) соответственно, р = 0,053.
Время поступления больных от начала болевого приступа до проведения ТЛТ в I группе – 23 (15,9%) и II – 26 (19,6%) различий не выявлено р = 0,4, 4/5 больных поступили до 6 часов в обеих группах.
Факторы риска. В нашем исследовании у пациентов одновременно имеется два и более факторов риска, что усиливает взаимное влияние их друг на друга: курение, артериальная гипертензия, сахарный диабет, гиперхолестеринемия и наследственность (табл. 1).
Локализация ИМ. В группе I и II передний –71 (49%) и 63 (47%), задний – 63 (43%) и 65 (49%), циркулярный 7 (5%) и 5 (4%) статистически не значимые межгрупповые различия. В группе I – 4 (3%) пациента с боковым ИМ. Класс тяжести у всех больных оценивался по Killip и Kimball. Класс Killip ? III в I –16 (11%) и II –18 (14%) пациентов.
Осложнения ИМ. Так, в I и II имели место: перикардит – 30 (20,7%) и 24 (18%), р = 0,5; ранняя постинфарктная стенокардия – в I и II – 11 (7,6%) и 10 (7,5%), р = 0,9. В 4 – 7% повторная ишемия приводит к развитию повторного ИМ. В I и II – 16 (11%) и 21 (15,8%), р = 0,2. В I и II развитие кардиогенного шока наблюдалось у 16 (11%) и 18 (14%), р = 0,4. Проявление острой левожелудочковой недостаточности – в I и II соответственно 24 (16,6%) и 16 (12%), р = 0,2.
Аневризмы сердца меньше в I,чем во II – 10 (6,9%) и 18 (13,5), р = 0,05, и у мужчин – 4 (2,8%) и 10 (7,5%), р = 0,07; у женщин – 6 (4,1%) и 8 (6,0%), статистически незначимо. Разрыв сердца, является второй по частоте непосредственной причиной смерти больных в стационаре. В I – 4 случая (2,8%) и вo II – 5 (3,6%), р = 0,6.
Таблица 1. Факторы риска в I и II группах
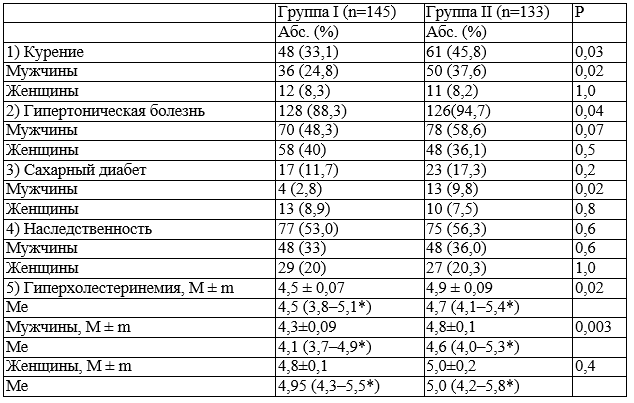
Примечания: M ± m – среднее значение (М) и стандартная ошибка среднего (m), Ме – медиана,* – 1-й – 3-й квартили распределения
Факторы риска и сопутствующая патология в группах умерших пациентов. В целом по группе I на 145 пролеченных больных 15 (10,3%) умерших, вo II на 133 – 14 (10,5%). В группах I и II – мужчин 9 (6,21%) и 8 (6,03%), р = 1,0 женщин – 6 (4,14%) и 6 (4,5%) р = 0,8. В обеих группах мужчин больше, чем женщин р = 0,4. В возрасте 60 – 74 г. г. умерших в I и II – 9 (6,21%) и 9 (6,76%), соответственно, р = 0,7 в возрасте 75 – 85 лет – 6 (4,14%) и 5 (4,27%), р = 1,0.
Среди умерших пациентов в обеих группах на первое место, по частоте встречаемости, выступила гипертоническая болезнь (ГБ) и дисциркуляторная энцефалопатия, которая отмечалась у всех. Распространенность артериальной гипертензии (АГ) среди населения велико: так в Российской Федерации около 40,4% АГ встречается среди женщин, среди мужчин – 37,2% [7]. В 70 % случаев в обеих группах умерших пациентов отмечалась хроническая сердечная недостаточность (ХСН) IIA в I и II – 11 (73,3%) и 10 (71,4%), ХСН II Б – 4 (26,7%) и 4 (28,6%) соответственно, р = 0,9.
ИБС, перенесенный ИМ в I и II – 2 (13,3%) и 3 (21,4%) р = 0,6. Сахарный диабет повышает риск развития ИБС в 2 – 4 раза, причем у женщин в большей степени, чем у мужчин. При использовании различных фибринолитических препаратов смертность от инфаркта миокарда среди больных с сахарным диабетом снижается так же, как и среди больных без диабета [9, 11, 13, 16]. В клинических испытаниях фибринолитиков при инфаркте миокарда, Fibrinolytic Therapy Trialists' (FTT) Collaborative Group отмечено, что в течение первых 35 суток у больных с диабетом смертность была несколько выше (21,7%), чем у больных без диабета (14,3%), однако различие оказалось статистически незначимым [11]. В этих испытаниях у больных с диабетом не наблюдалось увеличения частоты тяжелых кровотечений или инсульта [8, 9, 11]. Однако в эпоху тромболизиса внутрибольничная смертность среди больных с сахарным диабетом остается в 1,5–2 раза выше, чем среди больных без диабета. В исследовании TAMI (The Thrombolysis and Angioplasty in Myocardial Infarction) внутрибольничная смертность после инфаркта миокарда была почти вдвое выше у больных с диабетом; у этих больных чаще наблюдалась застойная сердечная недостаточность, а частота клинически подтвержденного повторного инфаркта была в 2 раза выше [9]. Аналогичные результаты получены в других крупномасштабных исследованиях [8, 10, 14, 15, 20]. И если, клинически верифицированный диагноз сахарный диабет в нашем исследовании I и II – 2 (13,3%) и 3 (21,4%) случаев, р = 0,5, то гипергликемия выявлена у всех умерших пациентов в I и II.
Более половины случаев у умерших пациентов выявлены курение и отягощенный анамнез по сердечно-сосудистым заболеваниям. Исследование INTERHEART показало, что курение 1 – 5 сигарет в день увеличивает риск развития ОИМ на 40%, что снижает эффект вторичной профилактики аспирином на 20% и статинами на 75% [19]. Так, курение в I и II – 8 (53,3%) и 3 (14,2%) р = 0,07 и наследственность в I и II – 9 (60%) и 6 (42,8%) р = 0,3.
В многочисленных эпидемиологических исследованиях доказано, что между повышенными уровнями в плазме крови общего холестерина, холестерина (ОХС) липопротеинов низкой плотности (ХС ЛПНП) и риском развития атеросклероза и ИБС имеется четкая положительная корреляция, тогда, как с уровнем холестерина липопротеинов высокой плотности (ХС ЛПВП) корреляция отрицательная, т.е. их повышенный уровень можно считать фактором антириска [4]. Риск развития ИБС, связанные с повышенным уровнем ОХС более выражены у молодых (< 55 у мужчин, < 65 у женщин) против старых, что составляет в 2,5 раза выше у молодых против старых [19]. Учитывая рекомендации ВНОК от 2009 г., оптимальные значения общего холестерина плазмы для больных с документированным атеросклерозом, лиц высокого и очень высокого риска осложнений атеросклероза (риск SCORE ? 5%, Sistemic Coronary Risk Evaluation) ? 4,0 ммоль/л. В нашем исследовании в I и II группах отмечалась гиперхолестеринемия – 4,45 ± 0,19 и 4,88 ± 0,39 соответственно, р = 0,5.
Выводы
1. Факторы риска такие, как курение, гиперхолестеринемия, отягощенная наследственность по сердечно-сосудистым заболеваниям являются предикторами ухудшающими прогноз заболевания независимо от применяемого тромболитического препарата.
2. Сочетание сахарного диабета и гипертонической болезни у пожилых пациентов с ОКСпST в группах при тромболизисе пуролазой в дозах 6–8 млн. МЕ и стрептокиназой в дозе 1,5 млн. МЕ утяжеляют состояние больного, и это может привести к летальному исходу.
