В течение последних лет в современной литературе, касающейся нефрологии и предикторов острого почечного повреждения, нейтрофильный желатиназно-ассоциированный липокалин (neutrophil gelatinase-associated lipokalin-2, NGAL) являлся предметом пристального изучения. Этот неослабевающий интерес продиктован уникальными свойствами данного протеина. NGAL принадлежит к семейству секретируемых липокалинов-сидерофоров, то есть способен транспортировать железо [6].
В зависимости от ряда условий и стрессирующих факторов, он способен синтезироваться различными иммунными клетками, адипоцитами, гепатоцитами, клетками почечных канальцев и эпителием пищеварительного тракта. Повышенный синтез липокалина в деградируемых тканях допускает его значение как фактора апоптоза с одной стороны, а с другой стороны, как фактора выживаемости клеток. Кроме того, вместе с микробными сидерофорами NGAL проявляет бактериостатическое действие и тормозит развитие инфекций. Благодаря этим свойствам липокалин, как и ряд других, эволюционно древних субстанций, участвует в острофазовом ответе на воспаление и повреждение [1,5].
Сердечно-сосудистая хирургия является одной из наиболее распространенных хирургических процедур. Острое почечное повреждение (ОПП) является часто встречающимся и серьезным послеоперационным осложнением после искусственного кровообращения (ИК), использующегося при неработающем сердце, с риском трансформации в хроническую почечную недостаточность (ХПН) [3,7]. Потребность в диализе у кардиохирургических больных с ОПП составляет 5%. Меньшая степень ОПП с увеличением креатинина более чем на 25% от исходных уровней к послеоперационному уровню наблюдается более чем у 50% пациентов [11]. Уровень мочевого NGAL (Urine NGAL, U-NGAL) может являться полезным прогностическим инструментом для определения риска ОПП, инициации заместительной почечной терапии (ЗПТ) и внутрибольничной летальности[10]. Вместе с тем, по данным мета- анализа установлено, что возраст является эффективным модифицирующим фактором уровня NGAL, с значительно лучшей предикативной способностью ОПП у детей чем у взрослых [4]. Кардиохирургические пациенты старше 65 лет представляет высокий риск развития послеоперационного ОПП, в силу имеющихся у них исходно сниженных биологических резервов, в том числе объема паренхимы почек. Ее функциональная способность регистрируется сниженной у данной популяции больных [9]. Научные работы, посвященные вариациям липокалина у пожилых пациентов немногочисленны [4]. Анализ влияния категорий кардиохирургических вмешательств (коронарное шунтирование, клапанная, комбинированная хирургия, реоперации) на секрецию мочевого NGAL ранее не проводился.
Цель исследования: изучение биологической вариации мочевого липокалина-2 у популяции пожилых пациентов, в зависимости от категории кардиохирургического вмешательства и операционных факторов.
Методика исследования. Проведено проспективное когортное исследование у 75 пациентов от 65 до 80 лет. Средний возраст составил 70,32 (межквартильный интервал 4). Из них 54,3% составили женщины и 45,7% мужчины европеоидной внешности. Критериями включения в исследование являлись: 1) возраст старше 65 лет, 2) кардиохирургическая операция в условиях ИК. Критерием исключения была смена вида операции на работающем сердце (без ИК). Кардиохирургические вмешательства, анестезиологическое пособие и ИК проводились согласно принятым в клинике стандартам. У 39 пациентов проведены шунтирующие миокард операции, 21- составили клапанные вмешательства. У 1 выполнено протезирование аорты, 14- составила комбинированная кардиохирургия. Повторная операция выполнена 4 больным. Материалом исследования явлалась моча из мочевого катетера непосредственно перед операцией и через 4 часа после кардиохирургического вмешательства. Моча забиралась шприцем в эпендорфы «Axygen genuine» (Axygen inc. USA) емкостью 150 мкл. Пробы хранились при температуре -800С с использованием низкотемпературного холодильника Snijders Hammerlit (Netherlands).
Анализ NGAL в моче проводился количественным определением на иммунохемилюминесцентном анализаторе Architect i2000sr (Abbott Laboratories, USA) с использованием набора «Urine NGAL» (Abbott Laboratories, USA) согласно инструкции производителя. Верификацию диагноза ОПП проводили согласно классификации RIFLE (2004), с учетом как степени прироста креатинина, так и темпа диуреза [9]. Стратификация производилась следующим образом: Risk-I, Injury-II, Failure-III степень соответственно.
Статистический анализ полученных данных был проведен в программах Excel из пакета Microsoft Office 2003, IBM SPSS Statistics 20.0.0. Результаты исследованы непараметрическими методами (медиана, 25-й и 75-й квартили); а также параметрическими (среднее и 95% ДИ для среднего). Дискриминационная способность показателей оценивалась с помощью ROC-анализа по величине площади под кривой – AUС. Оценка категорий и факторов риска проводилась с помощью робастного регрессионного анализа (М-статистика Хьюбера и волны Эндрюса). Статистически значимыми считались различия данных при р<0,05 для ошибок I рода (вероятность ложноположительных результатов), α<0,1 для ошибок II рода (вероятность ложноотрицательных результатов).
Результаты исследования. При анализе предикативной способности мочевого липокалина в развитии послеоперационного ОПП в сравнении с другими факторами кардиохирургического вмешательства у пожилых найдены определенные различия (табл. 1). По результатам ROC-анализа установлена «очень хорошая» (0,7-0,8) объясняющая способность как U-NGAL после операции, так и дельта U-NGAL, превышающая время операции и время ИК. Причем специфичность в определении ОПП у мочевого липокалина была выше, чем чувствительность, на что указывает низкая вероятность ошибки II рода (α=0,006) для дельта U-NGAL. Данная особенность может быть характерной для пожилых кардиохирургических пациентов.
Таблица 1. Сравнительная оценка валидности мочевого NGAL и факторов кардиохирургической операции в прогнозировании ОПП (RIFLE) у пожилых пациентов
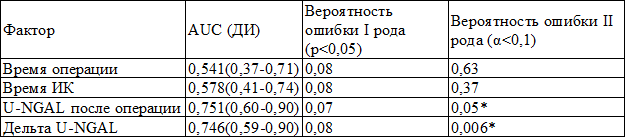
Примечание: ROC-анализ, статистически значимыми являлись результаты при p<0,05 и α<0,1 AUC-area under curve (площадь под характеристической кривой)
Для углубления исследования был проведен робастный анализ полиномиальной регрессии с использованием M-оценок Хьюбера, продублирован с использованием волны Эндрюса. Анализ категорий кардиохирургических операции как факторов риска ОПП с использованием в качестве предиктора мочевого NGAL, продемонстрировал отсутствие существенных дооперационных различий между ними (табл. 2). В сравнении с дооперационным уровнем, после вмешательства наблюдалось отчетливое возрастание U-NGAL, с существенным различием в ее степени между категориями оперативных вмешательств. В робастной модели регистрировалось возрастание уровня мочевого липокалина после шунтирования в 1,38, после операциях на клапанах сердца в 3,9 и после комбинированной хирургии в 13,2 раза соответственно, в сравнении и дооперационными значениями. Это может свидетельствовать о более выраженном операционно- перфузионном стрессе при увеличении сложности и травматичности сердечно-сосудистой операции. При этом увеличение продолжительности ИК было непропорционально меньшим, чем возрастание U-NGAL в соответствующих категориях. Это может свидетельствовать о преобладании фактора операционной агрессии в секреции липокалина. Также продемонстрировано статистически значимое развитие ОПП (Risk) в категории комбинированной кардиохирургии пожилых пациентов, с последующим исходом в хроническую болезнь почек (ХБП).
Таблица 2. Модель оценки мочевого NGAL и исследуемых факторов в зависимости от категории операции у пожилых кардиохирургических больных
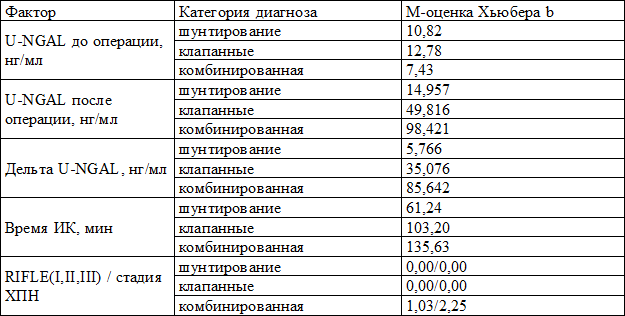
Примечание: M-робастные оценки (максимального правдоподобия) Хьюбера полиномиальной регрессии, b=1,339 - взвешивающая константа
Анализ зависимости повторного оперативного вмешательства на сердце и секреции мочевого NGAL продемонстрировал статистически значимые различия в исходном уровне (в 1,5 раза). В сравнении с дооперационным уровнем, после вмешательства наблюдалось возрастание мочевого NGAL, с существенными различиями в ее степени между первичными и повторными вмешательствами (табл. 3). Регистрировалось возрастание уровня липокалина мочи в 1,5-2 раза после первичной операции, и в 16-25 раз после повторных кардиохирургических вмешательств (при использовании различных робастных методов M-оценок). В исследуемой модели отмечалось частое развитие ОПП(Risk) после повторной операции, без последующей трансформации в ХПН у пожилых пациентов. Показано, что высокие уровни секреции мочевого NGAL у пожилых кардиохирургических пациентов сопровождаются большей частотой развития ОПП (AUC 0.75; ДИ 93% 0.60-0.90).
Таблица 3. Модель оценки мочевого NGAL и исследуемых факторов в зависимости от повторной операции у пожилых кардиохирургических больных
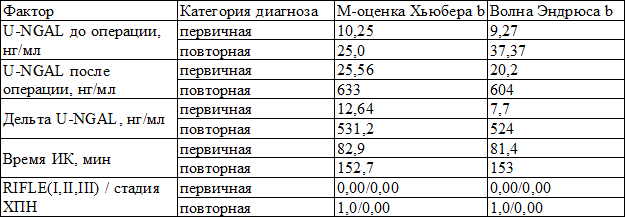
Примечание: M-робастные оценки (максимального правдоподобия) Хьюбера и волны Эндрюса полиномиальной регрессии, b -взвешивающая константа равна 1,339 для обоих методов, p<0,05 (ошибка I рода)
Выводы: установлены различия вариабельности секреции мочевого NGAL между категориями кардиохирургических вмешательств у пожилых пациентов после коронарного шунтирования, клапанных вмешательств, комбинированной хирургии и повторных операций (с дооперационным уровнем в 1,38; 3,9; 13,2 и 16 раз, соответственно).
