Введение. Сердечно-сосудистые заболевания (ССЗ) являются глобальной медико-социальной проблемой. Так, в России распространенность ишемической болезни сердца (ИБС) среди взрослого населения составляет 13,5% [6]. Особое место в лечении ИБС занимает хирургический метод реваскуляризации миокарда. При отсутствии положительного эффекта от медикаментозной терапии, доказанным высокоэффективным методом лечения является аортокоронарное шунтирование (АКШ). АКШ, основанное на методах реперфузии миокарда, является весьма эффективным, поскольку значительно снижает летальность и частоту развития осложнений, а также повышает качество жизни пациентов. Однако восстановление коронарного кровотока в ишемизированном миокарде, наряду с несомненным положительным эффектом, может оказывать и негативное действие, вызывая обратимые и необратимые реперфузионные повреждения и запуская неспецифический системный воспалительный ответ (СВО), который проявляется в форме постперикардиотомного синдрома (ПКТС) [1, 4]. ПКТС - это специфическая форма травматического перикардита, развивающаяся в рамках системной воспалительной реакции организма, сопряженной с нарушением редокс-гомеостаза и интенсификацией свободнорадикальных процессов [2, 11, 12].
Исследовали состояние глутатион-зависимой антиоксидантной системы (ГЗАС), вносящей существенный вклад в защиту клеток от деструктивного воздействия окислительного стресса и поддержание оптимального уровня свободнорадикального гомеостаза [8], в эритроцитах крови больных ИБС после прямой реваскуляризации миокарда.
Материал и методы. Обследовано 50 больных ИБС в возрасте 41-75 лет (58±1,5), которые перенесли аорто-коронарное шунтирование. Больные были разделены на 2 группы: 1 - больные ИБС, у которых в результате клинических исследований ПКТС не был установлен; 2 - больные ИБС, у которых был обнаружен ПКТС. Биохимические показатели исследованы в динамике: на 1-е, 3-е, 5-е, 7-е и 10-е сутки послеоперационного периода. В качестве контроля использовали кровь 20 практически здоровых людей обоего пола (доноры) в возрасте от 35 до 52 лет (средний возраст 46,2±0,7).
Материалами для биохимического исследования являлись эритроциты. Кровь собирали утром натощак из локтевой вены. В качестве антикоагулянта использовали К3-ЭДТА (этилендиаминтетрауксусная кислота) в концентрации 1,2 мг - 2,0 мг сухой ЭДТА на 1 мл крови. Кровь перед биохимическими исследованиями центрифугировали 10 мин при 3000 об/мин.
Для оценки состояния ГЗАС исследовали содержание восстановленного глутатиона (GSH), активность глутатионпероксидазы (ГПО), глутатионредуктазы (ГР) и глутатион-S-трансферазы (ГST). Содержание GSH оценивали по цветной реакции с 5,5-дитиобис-(2-нитробензойной) кислотой (ДТНБК, реагент Эллмана) с образованием соединения, которое обладает максимумом поглощения при 412 нм (ТНФА) [14]. Активность ГПО определяли по скорости окисления восстановленного глутатиона в присутствии гидроперекиси третичного бутила [3]. Метод определения активности ГР основан на ферментативном восстановлении окисленной формы глутатиона, интенсивность которого оценивается по степени окисления НАДФН при длине волны 340 нм [7]. Определение активности ГSТ основано на оценке скорости реакции ферментативного образования GS-2,4-динитробензола в реакции восстановленного глутатиона с 1-хлор-2,4-динитробензолом (ХДНБ) [15].
Статистическую обработку экспериментальных данных проводили с использованием t-критерия Стьюдента для малых выборок. Расчет производили с использованием программ «Statistica 10.0» и «Microsoft Excel». Достоверными считали различия при р<0,05. Резко отклоняющиеся варианты оценивали по критерию Шовене.
Результаты и обсуждение. Получены результаты, свидетельствующие о заметном повышении содержания GSH в течение всего исследованного периода в эритроцитах крови как у больных ИБС с клинически диагностированным ПКТС, так и у больных без данного синдрома (рис. 1). В 1-й группе уровень GSH возрастает от 31% до 43%, во 2-й группе - от 44% до 85% (p<0,05) относительно доноров. Причем, содержание GSH у больных с ПКТС выше, чем у больных без данного синдрома: на 7-е сутки - на 57%, на 10-е сутки - на 29% (p<0,05). Известно, что воспалительная реакция, развивающаяся в послеоперационном периоде у больных ИБС, сопровождается повышением продукции провоспалительных цитокинов и, в том числе, фактора некроза опухоли (ФНО). В свою очередь, сверхпродукция ФНО приводит к увеличению концентрации молекул межклеточной адгезии ICAM-1, которые способны модулировать экспрессию ключевого фермента биосинтеза глутатиона - глутаматцистеинлигазы [16], что может обуславливать прирост GSH (рис.1).
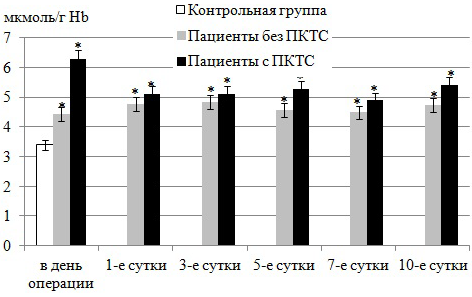
Рис. 1. Содержание GSH в эритроцитах крови больных ИБС, перенесших АКШ. Здесь и далее * отмечены статистически достоверные отличия по сравнению с донорами при р<0,05.
Установлено достоверное снижение на 23-39% активности ГПО в эритроцитах крови у больных ИБС без ПКТС в день операции и во все исследуемые сроки (рис.2). Динамика активности ГПО в эритроцитах крови больных с ПКТС не имеет статистически достоверных отличий по сравнению с донорами. Известно, что ГПО крайне чувствительна к изменению уровня пероксидов в системе, и их чрезмерная концентрация может приводить к ингибированию фермента [13], что наблюдается в 1-й группе больных.
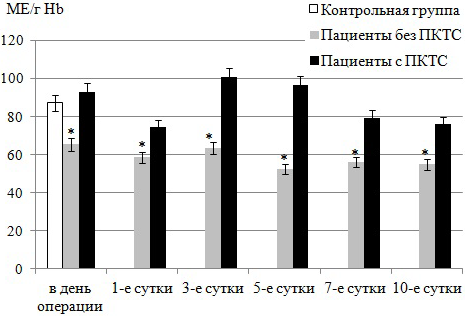
Рис. 2. Активность ГПО в эритроцитах крови больных ИБС, перенесших АКШ.
Установлено повышение активности ГР в эритроцитах обеих групп больных: в 1-й группе максимальное значение активности фермента наблюдается на 5-е сутки (возрастает на 411%) после оперативного вмешательства, а во 2-й - уже на 3-е сутки (возрастает на 562%) после операции (рис. 3). Исходя из полученных данных, можно предположить, что столь существенная активация ГР может быть связана с интенсивным расходованием GSH на непосредственную нейтрализацию активированных кислородных метаболитов, уровень которых существенно возрастает в крови больных ИБС, и опосредованное редокс-чувствительными белками (глутаредоксины) восстановление редокс-нарушений [9, 17]. В связи с этим возникает напряженность в работе ГР - фермента, ответственного за поддержание внутриклеточного пула GSH.
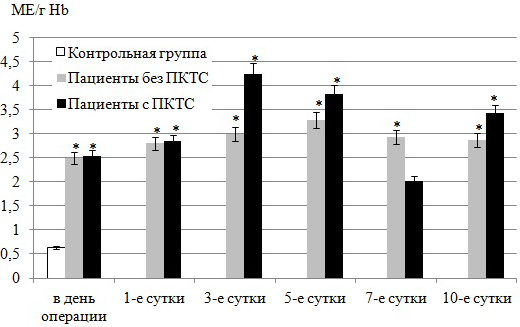
Рис. 3. Активность ГР в эритроцитах крови больных ИБС, перенесших АКШ.
Наблюдается существенная активация ГST, которая проявляет антиоксидантное действие посредством восстановления гидроперекисей липидов и конъюгации с GSH продуктов ПОЛ типа алкеналей, в обеих группах больных по сравнению с донорами (рис. 4). Активность ГST в эритроцитах больных без ПКТС возрастает на 193-207% с 1-х по 10-е сутки после операции с максимумом (прирост на 207%) на 5-е сутки. В то же время в эритроцитах больных с ПКТС активность ГST повышается на 148-308% и достигает максимального значения уже на 3-е сутки (прирост на 308%) после операции. Высокая активность ГST, возможно, объясняется усилением ПОЛ и накоплением в крови высокотоксичных реактивных карбонильных соединений (4-гидрокси-2-ноненаля, МДА и др.) и конечных продуктов липопероксидации (ALEs, advanced lipoxidation end-products), вызывающих необратимую модификацию клеточных структур [18]. ГST обладают высокой степенью сродства к GSH, поэтому даже небольшие колебания его уровня в эритроцитах очень точно отражаются на изменении активности ГST. Следует отметить, что активация ГST (в частности, ГSТO1-1, ГSТA1-1, ГSТM2-2) способствует цитотоксическому эффекту за счет ингибирования рианидиновых рецепторов сердечной мышцы (RyR2), ответственных за высвобождение Са2+ из внутриклеточных запасов [10].
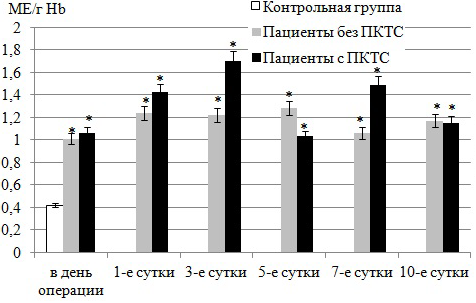
Рис. 4. Активность ГST в эритроцитах крови больных ИБС, перенесших АКШ.
Выводы:
Таким образом, полученные данные могут свидетельствовать о том, что прямая реваскуляризация миокарда, несмотря на терапевтическую эффективность, сопряжена с существенными изменениями редокс-гомеостаза в эритроцитах больных, которые, в свою очередь, могут повлиять на развитие послеоперационных осложнений. Обширное хирургическое вмешательство, при котором нарушаются нормальное потребление кислорода и образование энергии, обусловливает возникновение и развитие каскада патофизиологических реакций, основой которого является изменение процессов свободнорадикального окисления, т.е. происходит сдвиг динамического равновесия в сторону стимуляции образования активных кислородных метаболитов и накопления недоокисленных токсичных продуктов, способствующих усилению повреждающего действия [5].
Глутатионовая система имеет исключительно важное значение в регуляции редокс-потенциала кардиомиоцитов. В условиях свободнорадикального окисления изменения редокс-статуса имеют патологическую направленность и обуславливают усиление провоспалительных процессов в миокарде. Результаты исследования демонстрируют напряженность и дисрегуляция в работе глутатион-зависимых ферментов у больных с ПКТС. Ранние изменения динамики исследованных ферментов могут соответствовать быстрой форме ПКТС, развивающегося в течение первых семи суток после оперативного вмешательства.
Отдельно стоит подчеркнуть значимость глутатион-зависимой антикосидантной системы в мониторинге патологических изменений после кардиохиругического вмешательства. Дальнейшее исследование показателей ГЗАС в крови больных ИБС, перенесших аортокоронарное шунтирование, представляется перспективным для понимания механизмов развития послеоперационных осложнений и выбора наиболее эффективной постоперационной терапии пациентов.
