Актуальность. Медицинскую и социальную значимость проблемы диагностики, профилактики и лечения врождённых и наследственных заболеваний трудно переоценить. Одной из важных проблем современной перинатологии является рост врожденных пороков развития (ВПР). Популяционная частота пороков развития в различных странах, по данным Всемирной организации здравоохранения (ВОЗ), колеблется в пределах 2.7-16,3% [5].
Одной из важнейших проблем, находящихся на стыке интересов педиатров, детских хирургов и неврологов, является проблема лечения и реабилитации детей со спинномозговыми грыжами (СМГ) в силу неуклонного роста их частоты, тяжести течения и исхода. В структуре пороков невральной трубки СМГ составляют 65% и встречаются в 0,4-4,2 случаев на 1000 новорожденных [1, 3, 6, 10].
Наиболее неблагоприятными исходами спинномозговых грыж, и в медицинском, и в социальном плане, являются прогрессирующая гидроцефалия, периферические парезы и параличи нижних конечностей, тазовые расстройства в виде недержание мочи и кала, приводящие к инвалидизации детей [2, 5, 8, 11].
Не вызывает сомнение, что адекватная реабилитация и социальная адаптация больных этой группы в значительной степени зависит от своевременной диагностики и комплексного лечения всех имеющихся нарушений. Длительное и сложное лечение больных с пороками развития центральной нервной системы (ЦНС), необходимая медико-педагогическая коррекция дефектов и социальная помощь детям - инвалидам требует значительных моральных и экономических затрат [1, 2, 3, 7, 9].
Вопросы восстановления и компенсации нарушенных структур и функций спинного и головного мозга при СМГ являются наиболее актуальными.
Таким образом, изучение особенностей клинического течения, возможностей современных методов диагностики, определение оптимальных сроков и методов комплексного лечения и реабилитации детей с данным пороком развития на современном этапе является крайне актуальным и представляет большую научную и практическую значимость.
Цель исследования: изучить влияние комплексной терапии на электромиографические показатели при спинномозговых грыжах у детей.
Материалы и методы исследования: клинический материал, анализируемой в работе, представлен больными, находившимися на лечении в детских лечебно-профилактических учреждениях г. Ташкента (отделение плановой хирургии 2-й городской детской хирургической клинической больницы, отделение неонатальной хирургии Республиканского Перинатального Центра МЗ РУз, являющихся клиническими базами кафедры госпитальной детской хирургии ТашПМИ и отделение детской неврологии клиники ТашПМИ по диагностике и комплексному лечению 88 больных детей с СМГ в возрасте от одного дня до 12 лет).
Больные дети были разделены на две группы. В первую – группа сравнения вошли ретроспективный анализ 38 (43,2%) пациентов с СМГ, обследованных и лечившихся по традиционному способу. Во вторую - основную группу включены 50 (56,8%) детей с СМГ.
Распределение больных по возрасту и половой принадлежности, представлено следующим образом: среди больных больше всего младенческого возраста – до 12 месяцев (70 детей- 79,5%). Заметно меньше детей от 1 года до 3 лет (8 детей - 9,1%), и детей от 3 до 6 (6 детей – 6,8%), от 6 до 12 лет (4 детей- 4,5%). Среди наблюдавшихся больных преобладали мальчики - 45 (51,1%), патология среди девочек наблюдалось у 43(48,9%).
78 (88,6%) родились в срок, с массой тела от 2500 до 3501 гр. – 54 (61,4%), 3501 и больше – 24 (27,3%). 10 (11,3%) детей родились недоношенными в сроки беременности 34-36 недель.
Относительно позвоночного столба СМГ в области шейных позвонков наблюдалась у 2 (2,3%) больных, в области грудной клетки – у 2 (2,3%), поясничной области – у 38 (43,2%), крестцовой – 13 (14,8%), пояснично-крестцовой – у 33 (37,5%).
Поперечный размер грыжевого мешка колебался от 1,5 до 12 см. Соответственно размерам мы разделили грыжи на: малые с диаметром до 5 см - 34 (36,8±5,2%); средние с диаметром 5-10 см - 41 (46,6±5,3%); большие с диаметром более 10 см - 13 (14,8±3,8%) больных. Наиболее частая локализация (51; 57,9±5,3%) и большие размеры СМГ отмечалась в поясничном и пояснично-крестцовом отделе позвоночника.
У 29 (32,9±5,0%) больных грыжа была покрыта по всей поверхности нормальной кожей содержащие и подкожно-жировой слой, обеспечивающей ей надежную прочность и герметичность. У 28 (31,8±4,9%) больных грыжа была покрыта истонченной кожей или оболочкой. У 12 (13,6±3,7%) больных, особенно среди новорожденных детей с СМГ было обнаружено гнойное или гнойно-фибринозное воспаление грыжевой оболочки, у 10 (11,4±3,4 %) грубые рубцовые изменения, у 9 (10,2±3,2%) ребенка отмечался разрыв грыжевой оболочки. Именно истончения или разрыв оболочек СМГ послужили переводу новорожденных или детей грудного возраста в хирургическую клинику по срочным показаниям к оперативному вмешательству.
Клинико-морфологические формы СМГ у наблюдавшихся больных представлены в табл. 1.
Таблица 1. Клинико-морфологические формы СМГ
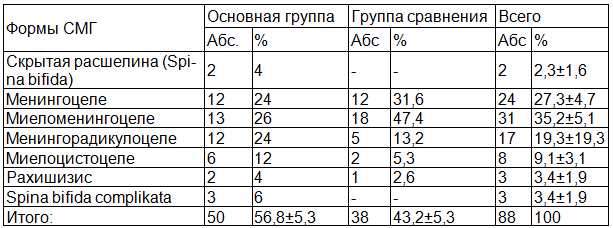
Значительно преобладала 83 (94,3±2,5%) кистозная форма заболевания, скрытая расщелина с явными признаками нарушения функции тазовых органов наблюдали у 2 (2,3±1,6%) больных, полный рахишизис диагностированы у 3 (3,4±1,9%) больных. Среди морфологических форм заболевания с вовлечением в процесс спинного мозга или его корешков наблюдался в 62 (70,5±4,9%) случаев.
При кистозной расщелине среди больных основной группы в 3 (3,4±1,6%) случаев имела места Spina bifida complicata — незаращение дуг позвонков, сочетающееся с разрастаниями жировой и фиброзной ткани – липоменингоцеле (1; 1,1±1,1%), а также тератоидными образованиями (3; 3,4±1,9%).
Сроки госпитализации и возраст больных на оперативное лечение были установлены в зависимости от размеров грыжи и состояния грыжевого покрова, течение болезни и характера осложнений. Новорожденные дети с СМГ в хирургический стационар были доставлены в течение первой недели жизни – 14 (15,9±3,9%), второй недели – 4 (4,5±2,2%), третьей недели – 2 (2,3±1,6%), четвертой недели – 1 (1,1±1,1%) и 49 (55,7±5,3%) детей в грудном возрасте, в 18 (20,5±4,3%) случаев в возрасте 3-12 лет.
Анамнестическое изучение течение беременности и перинатального периода жизни детей со СМГ не позволило четко выделить доминирующую причину возникновения порока, установлено значение различных эндогенных и экзогенных факторов.
По показателям физического развития больные дети с СМГ в 69,3±4,9% (61 ребенок) случаях отставали от сверстников. Нормальное физическое развитие отмечено у 26,2±4,7% (23 больных), у 4,5±2,2% (4) обследованных отмечено явления паратрофии.
Различные сопутствующие заболевания как пневмония у 7 (7,9%), внутриутробная инфекция с поражением внутренних органов у 9 (10,2%), родовая черепно-спинальная травма у 12 (13,6%) или сопутствующие пороки развития: аномалия развития мочевыводящих путей у 10 (11,4%), желудочно-кишечного тракта (ЖКТ) - 1 (1,1%); ЦНС - 3 (3,4%) больных отягощали течение СМГ.
Состояние обследованных детей при поступлении было оценено как тяжелое в 21 (23,9%) случаях; средней тяжести - в 56 (63,6%) и у 11 (12,5%) больных состояние расценено как удовлетворительное.
Оперативное лечение проводилось у 74 (84,1%) из 88 больных. Из них 42 (56,8%) были оперированы в возрасте 1-28 дней, 20 (27%) - от 1 месяца до 1 года, 12 (16,2%) - 1- 12 лет.
14 (15,9%) детям: (6 – 42,9%) из контрольной и (8 -57,1%) из основной группы) оперативное вмешательство не проводилось.
Девять (64,3%) детей были признаны неоперабельными из-за наличия тяжелых сопутствующих заболеваний и множественных сочетанных врожденных пороков развития. В 3 (21,4%) случаях родители отказались от оперативного вмешательства, из-за явного неблагоприятного прогноза. Двое (14,3%) больных из основной группы при скрытой СМГ не нуждались в оперативном вмешательстве, у них проводилось консервативное лечение.
В группе сравнения до проведения оперативного вмешательства были проведены традиционные методы исследования. В данной группе при оценке отдаленных результатов лечения проводилась комплексное исследование, идентичное основной группе, где клинические, параклинические, инструментальные и лабораторные методы проведены в динамике: до и после проведенного лечения.
При клиническом осмотре оценивали общее состояние, учитывали факторы, обусловливающие тяжесть состояния больного и отягощающие течение СМГ. Оценены также локализация грыжевого выпячивания по позвоночному столбу, его вид, размеры и состояние грыжевых оболочек. Каждого ребенка с СМГ проверяли на сопутствующие заболевания и пороки развития других органов и систем.
Электронейромиография (ЭНМГ) нижних конечностей проведена в неврологической клинике «Global Med System» 28 (56%) больным основной группы. Проводилась методика глобальной ЭНМГ на 4-х канальном электронейромиографе «Нейро-МВП-4» компании Нейрософт (Россия).
Для определения характера поражения нервов нижних конечностей и оценки состояния мотонейронального пула передних рогов спинного мозга обследовали большеберцовый нерв справа и слева. Определяли 3 основных ЭНМГ параметра – скорость распространения возбуждения по моторным волокнам (СРВм), моторный ответ (М ответ) и регистрацию F волн - возбуждение мотонейронов (наличие блоков).
Всем детям с СМГ в послеоперационном периоде проводили восстановительную терапию, включавшую медикаментозное и физиотерапевтическое воздействия, направленные на предупреждения развития спаечного процесса, рассасывания спаек, улучшения кровообращения, облегчения проведения нервных импульсов и восстановление функции нейромышечного аппарата. Курс лечения составлял 15-20 дней в течение 2 лет каждые 3-4 месяца, а в последующем – 2 раза в год.
При гипорефлекторной дисфункции проводили курс стимуляции детрузорной активности мочевого пузыря нивалином внутримышечно в течение 10 дней, в последующем в виде таблеток продолжительностью 30-40 дней. Детям в возрасте до одного года проводили электрофорез с нивалином в область мочевого пузыря.
При гиперрефлекторной дисфункции и детрузорно - сфинктерной дессинергии в комплекс медикаментозной терапии включали: М-холинолитики, атропин путём электрофореза на область мочевого пузыря по 5 дней; седативную терапию перед сном (биопассит, новопассит, пустырник) в возрастной дозировке.
Результаты исследования: электромиографические исследование, отражающие состояние функции мышц конечности на этапах хирургического лечения СМГ проведены у 28 больных до и после проведения оперативного вмешательства.
Важным показателем состояния нервно-мышечного аппарата служит М-ответ. У детей с СМГ данный показатель был достоверно ниже как по n.tibialis D, так и n.tibialis S и отличался от цифр контрольной группы почти в 2,5 раза (Р<0,001).
Скорость распространения возбуждения по нерву (СРВ) так же была достоверно снижена по сравнению с показателями контрольной группы с обеих сторон и составила 32,5±2,5 и 34,5±2,2 против 44,8±1,4 и 45,4±1,3 соответственно (Р<0,001) (табл. 2).
Таблица 2. Электронейромиографические показатели обследованных детей
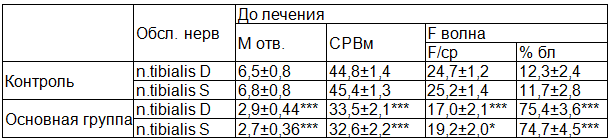
Примечание: * - достоверность данных по сравнению с контролем (*- Р<0,05; ** - Р<0,01).
Показатели F волны по большеберцовому нерву, после непрямой супрамаксимальной стимуляции мышцы появляется через десятки миллисекунд после М-ответа. По нашим данным, они достоверно отличались от контрольных цифр (Р<0,001), что характерно для корешкового поражения.
ЭНМГ заключения у 25% (7) больных детей выявили выраженные корешково - мотонейральные поражения на уровне L4-S1; снижение возбуждения мотонейрального пула - у 64,3% (18) детей с СМГ. Корешковые поражения зарегистрированы у 5 детей (17,9%). У 46,4% (13) детей наблюдалось аксональное поражение длинных нервов нижних конечностей.
Таким образом, у всех детей с СМГ отмечены нарушения двигательной активности мышц в нижних конечностях по большеберцовому нерву.
Полученные результаты ЭНМГ исследований у 28 (56%) больных, после проведенных оперативных вмешательств и комплексной терапии доказывали эффективность выбора проведенных лечебных мероприятий (табл. 3).
Таблица 3. Показатели ЭНМГ у детей с СМГ после комплексной терапии, n =28
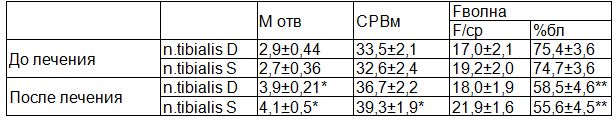
Примечание: * - достоверность данных по сравнению с показателями до лечения и после лечения (* - Р<0,05; ** - Р<0,01).
Полученные данные свидетельствуют о положительной динамике восстановления проводимости биоэлектрических потенциалов по большеберцовому нерву в 85,7%, улучшении двигательной активности в нижних конечностях у детей с СМГ.
Таким образом, ЭНМГ исследования, проведенные у 28 (56%) больных с СМГ, после проведенных оперативных вмешательств и комплексной терапии доказывали эффективность выбора проведенных лечебных мероприятий.
Выводы
1. Данные ЭНМГ повышают точность комплексной диагностики, позволяют оценить динамику функциональных нарушений и прогноз заболевания у детей с СМГ.
2. Доказана целесообразность ЭНМГ в выявлении поражений двигательной активности мышц в нижних конечностях по большеберцовому нерву, от которых зависит течения и прогноз болезни у детей с СМГ.
3. Анализ результатов лечения при СМГ показал целесообразность проведения целенаправленного комплексного лечения, позволяющего улучшить двигательную активность мышц в нижних конечностях, что предупреждает развитие вторичных органических изменений.
