Актуальность. Рациональное питание детей играет ключевую роль в обеспечении их гармоничного роста, физического и нервно-психического развития, устойчивости к воздействию инфекций и других неблагоприятных факторов внешней среды [4, 7]. Пищевая аллергия является одной из распространенных медицинских проблем детского возраста. Большое значение в педиатрической практике имеет ее своевременная диагностика, поскольку, начавшись с кожных или гастроинтестинальных симптомов, пищевая аллергия в дальнейшем может привести к развитию более тяжелых заболеваний, таких как аллергический ринит и бронхиальная астма. В связи с этим остается открытым вопрос правильного введения продуктов прикорма ребенку первого года жизни [1, 2, 5, 6].
Цель: изучить клинические признаки аллергических реакций у детей с пищевой аллергией после введения продуктов прикорма.
Материалы и методы. В исследовании приняли участие 40 детей в возрастной категории 4-7 месяцев жизни, имеющих отягощенный аллергологический анамнез (признаки пищевой аллергии легкой степени выраженности), не получавших ранее продукты прикорма. От родителей пациентов получено информированное согласие на участие в исследовании.
Согласно рекомендациям «Национальной программы оптимизации вскармливания детей первого года жизни в Российской Федерации» от 2011 г. всем детям введение прикорма проводилось поэтапно, с постепенным расширением ассортимента продуктов по мере роста ребенка, в количестве, соответствующем его возрасту [3]. Каждый новый продукт вводился в течение 10-14 дней. Всем пациентам были предложены продукты прикорма по 8-10 наименований каждому ребенку. В качестве контроля использовали клинические показатели наблюдаемых детей в течение всего периода исследования.
Используемые продукты для детского вскармливания (фруктовые пюре, безмолочные каши, детские овощные пюре, мясные пюре) изготовлены из натурального экологически чистого сырья, без применения консервантов, ароматизаторов, красителей, сахара, загустителей; не содержат генетически модифицированных продуктов; обогащены необходимыми минеральными веществами и витаминами; содержат достаточное количество питательных веществ, необходимых для роста и развития ребенка. Продукты соответствуют всем требованиям государственных стандартов и рекомендованы к использованию в питании детей первого года жизни.
Все пациенты были разделены на две группы в зависимости от возраста введения первого прикорма. В первую группу вошли дети, которые начали получать прикорм с 4,5 мес. Вторую группу составили пациенты, которые стали получать прикорм в возрасте 5 мес.
Также каждая группа была разделена на две подгруппы. Подгруппа А - дети, которые в качестве первого прикорма получали овощное пюре. Подгруппа В - дети, которым в качестве первого прикорма вводили кашу. Последовательность введения продуктов прикорма детям разных групп и подгрупп отражена на рис. 1 для первой группы и рис. 2 для второй.
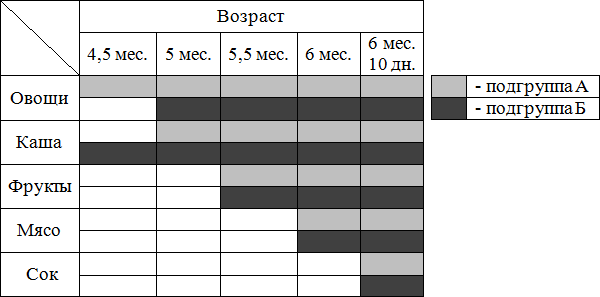
Рис. 1. Последовательность введения продуктов прикорма детям первой группы.
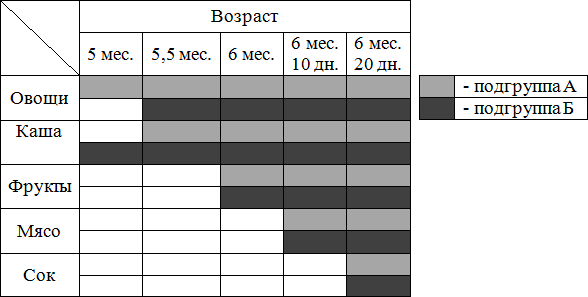
Рис. 2. Последовательность введения продуктов прикорма детям второй группы.
Результаты. Перед началом исследования у всех детей провели клиническое обследование, где определили частоту признаков диспепсии: у 17,5% (n=7) детей отмечалось снижение аппетита, приблизительно у такого же количества (n=8; 20%) - срыгивания, у 10% (n=4) наблюдался метеоризм, колики - в 13% случаев (n=5), запоры - у 7,5% пациентов (n=3).
В большинстве случаев дети хорошо отнеслись к предлагаемым продуктам прикорма и не отказывались от их приема, что отражено на рис. 3.
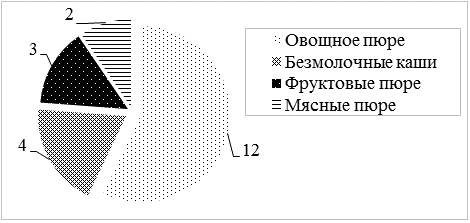
Рис. 3. Переносимость вводимых продуктов прикорма детей первого года жизни.
Из рис. 3 видно, что 30% (n=12) детей поначалу с неохотой ели овощное пюре (брокколи, цветная капуста и тыква), 10% (n=4) пациентов гречневую и рисовую кашу, 7,5% из них - пюре и сок из яблок и груши (n=3), и лишь 5% детей мясное пюре из кролика и индейки (n=2). Это можно объяснить изменением консистенции и вкуса новой пищи.
Изменений общего состояния детей, признаков аллергических реакций после приема исследуемых продуктов не отмечено. Что касается функциональных нарушений пищеварительной системы, то у отдельных детей в первые три дня наблюдались срыгивания, кишечная колика, метеоризм, задержка стула, что можно определить как реакцию организма на новый вид пищи (рис. 4 и 5).

Рис. 4. Частота проявлений диспепсических расстройств у детей после введения новых продуктов прикорма (фруктовых соков и пюре).
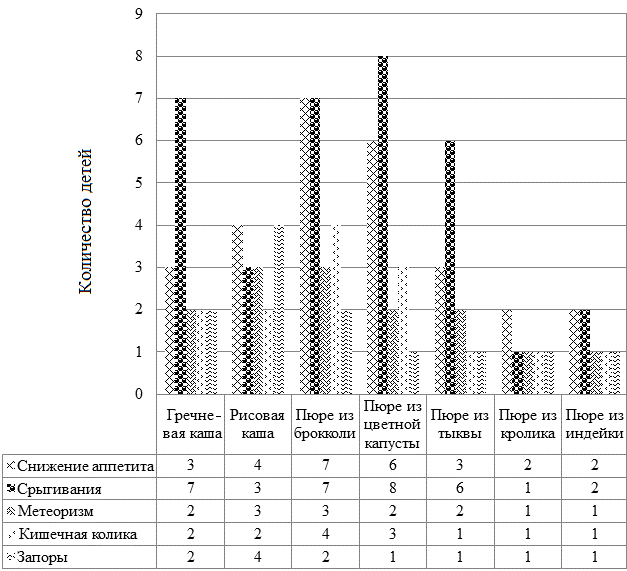
Рис. 5. Частота проявлений диспепсических расстройств у детей после введения новых продуктов прикорма (безмолочных каш, овощных и мясных пюре).
Анализируя данные рис. 4 и 5, следует сделать вывод, что наибольшая частота возникновения симптомов диспепсии регистрировалась после приема овощных пюре, наименьшая - после фруктовых соков.
Также всем пациентам проводили копрологическое исследование для оценки усвояемости продуктов прикорма, результаты которого представлены на рис. 6.
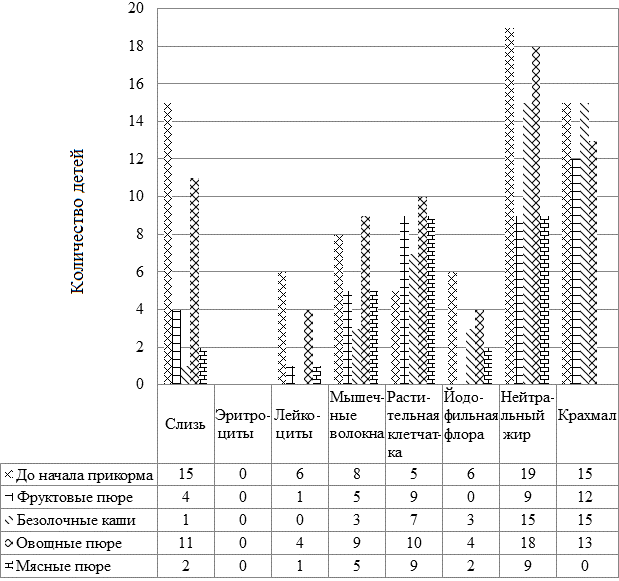
Рис. 6. Результаты копрологического исследования у детей после начала прикорма.
Из данных рис. 6 мы установили, что после введения продуктов прикорма у детей изменились показатели копрограммы. Отмечалось снижение содержания слизи, лейкоцитов, йодофильной флоры, нейтрального жира, крахмала. Это доказывает хорошую перевариваемость, усвоение фруктовых, овощных, мясных пюре, безмолочных каш.
Следующим этапом стало клиническое обследование детей на предмет наличия у них кожных проявлений аллергии, а именно сухости и гиперемия кожи, которая была обнаружена у 15% пациентов (n=6) и единичных папулезных высыпаний - в 25% случаев (n=10). Полученные результаты отражены на рис. 7.

Рис. 7. Распространенность кожных признаков пищевой аллергии у детей после начала прикорма.
Далее мы изучили уровень специфических иммуноглоулинов класса Е (IgЕ) к исследуемым продуктам прикорма. Уровни специфических IgE (кЕ/л) к изучаемым продуктам прикорма на начало и завершение исследования представлены на рис. 8.

Рис. 8. Уровень специфических IgE (кЕ/л) к изучаемым продуктам прикорма на начало (дробь) и завершение (косая полоса) исследования.
Из рис. 8 видно, что все показатель находятся в переделах возрастной нормы (сенсибилизации не выявлено).
Выводы. Таким образом, в ходе исследования выяснили, что после введения прикорма частота встречаемости функциональных нарушений пищеварительной системы уменьшилась; новых кожных проявлений пищевой аллергии не наблюдалось, а у детей, ранее их имевших, отмечалось значительно улучшение состояния кожных покровов.
