Введение. Химия анальгетических и противовоспалительных средств является одной из динамически развивающихся отраслей химической науки, что обусловлено практической значимостью этих соединений. Анальгетические и противовоспалительные средства представляют собой обширную и разнообразную по химическому строению группу лекарственных средств, широко применяющихся в клинической практике. Большинство препаратов этой группы, относятся по современной терминологии к "кислотным" противовоспалительным средствам. Им присущи и сходные побочные эффекты: повреждающее действие на слизистую оболочку желудочно-кишечного тракта, нарушение функции почек и некоторые другие.
Производные кислот вошли в клиническую практику и повсеместно применяются до настоящего времени. Такие производные как кислота ацетилсалициловая, кетопрофен, ибупрофен, напроксен, флурбипрофен используются в медицине в качестве анальгетиков, антипиретиков и противовоспалительных средств. В связи с этим, актуальным остается поиск новых веществ, отличающихся повышенной биологической активностью в сочетании с низкой токсичностью и менее выраженным побочным действием.
Целью настоящего исследования явилась оценка анальгетической активности новых производных тиадиазола при химическом болевом раздражении у крыс.
Материалы и методы. Исследования проведены с использованием 40 белых неинбредных крыс обоего пола массой 220±10 г. Подопытных животных содержали в условиях вивария (с естественным режимом освещения; при температуре 22-240; относительной влажности воздуха 40-50%) с использованием стандартной диеты (ГОСТ Р 50258-92). Эксперименты проводили в соответствии с правилами качественной лабораторной практики (GLP) при проведении доклинических исследований в РФ [1], а также правилами и Международными рекомендациями Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях (1986) [2]. Перед постановкой эксперимента животные проходили карантин в течение 10-14 дней [3, 4].
Исследуемые соединения перед опытом растворяли в воде очищенной и вводили внутрижелудочно в объеме 50мг/кг веса животного за 30 мин до введения уксусной кислоты. Животным контрольной группы внутрибрюшинно вводили изотонический раствор NaCl. У подопытных животных вызывали химическое раздражение брюшины (тест "корчей") путем внутрибрюшинного введения уксусной кислоты в концентрации 1% в объёме 1 мл/100 г веса животного. Регистрировали число специфических ноцицептивных ответов типа "корчи", возникающих в ответ на введение химического раздражающего агента и проявляющихся характерными потягиваниями. Анальгетическое действие оценивали по уменьшению числа "корчей" за период регистрации данной поведенческой реакции. Препараты вводили внутрижелудочно за 30 минут до введения кислоты.
Оценивали обезболивающую активность двух новых производных тиадиазола с лабораторными шифрами ЛХТ 3-10 и ЛХТ 10-10, синтезированных в ОАО «Всероссийский научный центр по изучению биологически активных веществ» (ВНЦ БАВ, Россия, Старая Купавна). Исследуемые соединения вводили внутрибрюшинно в терапевтической дозе равной 1/20 LD50 (50 мг/кг). Значение LD50 рассчитывали по данным токсикологических исследований. В качестве препарата сравнения использовали кетопрофен.
Учитывая тот факт, что многие НПВС оказывают ульцерогенное действие, нами была проведена оценка ульцерогенной активности новых производных тиадиазола. С этой целью исследуемые вещества (в виде растворов или водных суспензий с 1% раствором крахмала) вводили однократно в течение 4 дней внутрижелудочно крысам, лишенным пищи за 16 часов до опыта. Через 3 часа животных забивали, извлекали желудки, рассекали по малой кривизне и промывали в физиологическом растворе для удаления содержимого. Оценку ульцерогенного эффекта проводили по 4-х бальной шкале: 0 – отсутствие повреждений; 0,5 – гиперемия; 1 – единичные незначительные повреждения (1 – 2 точечных кровоизлияний); 2 – множественные повреждения (эрозии, точечные кровоизлияния); 4 – грубые повреждения, охватывающие всю поверхность слизистой (массивные кровоизлияния, эрозии, перфорации).
Результаты исследования обработаны статистически с применением стандартного пакета программ Microsoft Office Excel 2003. Для ряда выборок вычисляли среднюю арифметическую и среднюю квадратическую ошибку. Определение нормальности распределения переменных проводили на основании гистограмм распределения, величины асимметрии и эксцессы. Для оценки достоверности различий выборок, имеющих нормальное распределение, применяли параметрический t-критерий Стьюдента. За достоверное принимали различие при уровне вероятности 95% и более (p <0,05).
Результаты и их обсуждение. Анализ результатов экспериментов по оценке анальгетической активности показал, что новые производные тиадиазола с лабораторными шифрами ЛХТ 3-10, ЛХТ 10-10 обладают способностью уменьшать выраженность специфических ноцицептивных ответов у крыс при химическом раздражении брюшины (табл. 1). Отмечено, что при внутрибрюшинном введении 1% раствора уксусной кислоты (1 мл/10 0г) у всех подопытных животных возникали «уксусные корчи» (характерные движения животных, включающие сокращение брюшинных мышц, чередующиеся с их расслаблением, вытягиванием задних конечностей и прогибанием спины).
Таблица 1. Влияние производных тиадиазола и кетопрофена на число специфических ноцицептивных ответов на химическое раздражение брюшины у крыс.

Примечание: * - различия с контролем достоверны (p<0,05)
У животных группы контроля, получавших изотонический раствор NaCl, число специфических ноцицептивных ответов на внутрибрюшинное введение уксусной кислоты составило 34,9 корчей/час. При внутрибрюшинном введении нестероидного противовоспалительного средства кетопрофена (50 мг/кг) число «уксусных корчей» у подопытных крыс было в среднем в 1,2 раза (p<0,05) меньше, чем в контроле.
Обращает на себя внимание тот факт, что новые соединения, являющиеся производными тиадиазола, также обладали способностью уменьшать число специфических ноцицептивных ответов на химическое раздражение брюшины у подопытных животных. Было отмечено, что при внутрижелудочном введении соединений с лабораторными шифрами ЛХТ 3-10 (50 мг/кг) и ЛХТ 10-10 (50 мг/кг) число «уксусных корчей» было в среднем на 1,2 раза (р<0,05) меньше, чем в контроле (подопытные животные, получавшие изотонический раствор натрия хлорида). Приведенные данные показывают, что активность новых производных тиадиазола (ЛХТ 3-10 и ЛХТ 10-10 в дозе 5% от LD50) в этом отношении была сопоставима с активностью кетопрофена (50 мг/кг). Достоверных различий в эффективности соединений ЛХТ 3-10 и ЛХТ 10-10 отмечено не было.
На следующем этапе экспериментальных исследований оценивали изменения слизистой оболочки желудка у крыс, получавших внутрижелудочно производные тиадиазола. Анализ результатов экспериментов при внутрижелудочном введении нестероидного противовоспалительного средства индометацина в дозе 50мг/кг у подопытных крыс развивались выраженные изменения слизистой оболочки желудка, анализ показал, что производные тиадиазола под лабораторными шифрами ЛХТ 1-10, ЛХТ 3-10, ЛХТ 10-10, ЛХТ 12-10, ЛХТ 14-10 влияют на целостность слизистой желудка (табл. 2).
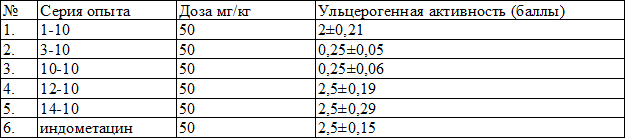
Соединения ЛХТ 3-10 и 10-10, не вызывали значительных повреждений слизистой желудка, иногда наблюдалась легкая гиперемия. ЛХТ (1-10, 12-10, 14-10, индометацин) вызывали повреждения слизистой в виде эрозий, язв, и кровоподтеков. Наибольшие повреждения виде язв и эрозий наблюдались после воздействия индометацина, ЛХТ 12-10 и ЛХТ 14-10. Умеренные повреждения слизистой оболочки виде эрозий и кровоподтеков наблюдались у препарата ЛХТ 1-10.
Таблица 2. Выраженность ульцерогенного действия новых производных тиадиазола и индометацина при внутрижелудочном введении у крыс
В последние годы сформировалась новая точка зрения на механизмы повреждения слизистой ЖКТ. Многие исследователи считают, что этот механизм комплексный и обусловлен не только торможением нестероидными противовоспалительными препаратами синтеза простагландинов и нарушением синтеза мукополисахаридов, но и снижением разности трансмукозного потенциала в желудке и повышением обратной диффузии ионов H+, а в кислой среде – проницаемости апикальных мембран слизистой желудка может быть только предпосылкой для формирования повреждений, но одного этого механизма недостаточно для развития повреждений, вызываемых ацетилсалициловой кислотой. В механизме ульцерогенного действия НПВП определенную роль играет и повышение интенсивности перекисного окисления липидов. Образующиеся в результате действия НПВП продукты свободно-радикального окисления принимают участие в поражении ЖКТ, а также могут участвовать в разрушении мукополисахаридов. Есть данные литературы, показывающие, что антиоксиданты уменьшают повреждающее действие НПВП (АСК, индометацина и др). Противоязвенный эффект витамина С, α-токоферола, метилурацила обьясняют именно антиоксидантным механизмом [5].
Следует отметить, что в структуру новых производных тиадиазола входят янтарная (ЛХТ 10-10) и пиколиновая (ЛХТ 3-10) кислоты, придающие соединениям антиоксидантные свойства, что, возможно имеет значение для реализации их фармакологической активности. Таким образом, результаты экспериментального исследования показали, что среди производных тиадиазола имеются низкотоксичные соединения, обладающие анальгетической и противовоспалительной активностью.
Выводы
1. Среди производных тиадиазола имеются соединения с выраженной анальгетической активностью.
2. Новые производные тиадиазола ЛХТ 3-10 и ЛХТ 10-10 при внутрижелудочном введении подопытным мышам в дозе 5% от LD50 (50мг/кг)уменьшали количество специфические ноцицептивных ответов на химическое раздражение брюшины у подопытных животных в среднем на 1,2 раза (р<0,05) по сравнению с контролем.
3. Обезболивающая активность новых производных тиадиазола ЛХТ 3-10 и ЛХТ 10-10 при внутрибрюшинном введении мышам в дозе 5% от LD50 соответствовала эффектам кетопрофена (50 мг/кг)
4. Ульцерогенной активности у новых производных тиадиазола под шифрами ЛХТ 3-10 и ЛХТ 10-10 не наблюдалось.
