Открытие и исследование механизмов действия новых эффективных фармакологических субстанций, потенциальных лекарственных препаратов (ЛП) является одной из основных задач современной фармакологии и медицины в целом. На Европейском Севере России особый интерес с точки зрения природного ресурсоведения и фармакоэкономики представляют гидробионты Белого и Баренцева морей, в частности, ламинария (Laminaria saccharina) - источник альгиновой кислоты, нейтральных полисахаридов (ламинарин), сульфатированных полисахаридов (фукоидан), многоатомных спиртов (маннит) и др., обладающих значимой фармакологической активностью. Сложившаяся ситуация открывает перспективу углубленного исследования фармацевтической субстанции на основе регионального биоресурса - морской бурой водоросли ламинарии (Laminaria saccharina) и изучения ее пролиферативного потенциала.
Разработана оригинальная методика энзиматической деструкции альгиновой кислоты, позволившая уменьшить молекулярную массу и снизить степень полимеризации данного соединения. Полученная субстанция была стандартизирована по количественным показателям, определенным в ходе проведения ядерно-магнитной резонансной спектроскопии и эксклюзионной высокоэффективной жидкостной хроматографии.
Цель работы - изучение пролиферативной активности оригинальной фармацевтической субстанции на основе деструктурированной натриевой соли альгиновой кислоты на модели раневого процесса в эксперименте и определение фармакокинетических показателей оригинальной субстанции при местном применении.
Методика исследования. Экспериментальное исследование выполнено на базе кафедр фармакологии, оперативной хирургии и топографической анатомии ГБОУ ВПО «Северный государственный медицинский университет» (г. Архангельск) Минздрава России. Экспериментальное моделирование раневого процесса на лабораторных животных осуществлено в асептических условиях учебной операционной кафедры оперативной хирургии и топографической анатомии, там же осуществлялось наблюдение за животными.
Эксперименты выполнялись с соблюдением современных требований к проведению исследований на лабораторных животных [1,6,8,10] и одобрены локальным Этическим комитетом ГБОУ ВПО «СГМУ» (Протокол № 01/1-13 от 27.02.2013 г.).
В ранее проведенных исследованиях [2] была выявлена эффективная доза деструктурированной альгиновой кислоты равная 2 мг/мл, определена молекулярная масса, которая составила 5,15 кДа, а также уставлена безопасность применения данного соединения.
На основе образца оригинальной фармацевтической субстанции, полученной энзиматической деструкцией, были изготовлены конъюгаты с флуоресцеином (флуоресцеин-5-изотиоцианат).
Лабораторные животные белые беспородные крысы-самцы весом 200±20 г в количестве 20 особей (питомник «Рапполово», Ленинградская область, Всеволжский район, поселок Рапполово) были разделены на 2 группы (табл. 1) и получали раствор «меченной» альгиновой кислоты в течение 7 дней. Формирование плоскостной асептической раны осуществлялось по методике Д.В. Королева [4].
У животных, в условиях наркотизации диэтиловым эфиром, на предварительно депилированной коже спины, после обработки операционного поля йодопироном и 70% спиртом стерильным скальпелем формировалась плоскостная округлая рана диаметром 1 см. Стандартизация полученной кожно-фасциальной раны была соблюдена путем применения трафарета из тонкого оргстекла (2 мм), в котором было сделано отверстие диаметром 1 см. Для формирования одинаковых по глубине ран использовался ограничитель. Животные выводились из эксперимента на 7-е сутки путем применения диэтилового эфира в летальных дозах.
Таблица 1. Разделение лабораторных животных на группы

Результаты оценивались методом обзорной флуоресцентной микроскопии. Затем была осуществлена окраска гистопрепаратов гематоксилин-эозином и вновь были выполнены исследования в условиях флуоресценции.
Оценка пролиферативной активности деструктурированной альгиновой кислоты проводилась на 7-е сутки эксперимента, что соответствует пролиферативной фазе раневого процесса [7]. Эксперимент выполнен на лабораторных животных белых беспородных крысах-самцах весом 200±20 г в количестве 50 особей (питомник «Рапполово», Ленинградская область, Всеволжский район, поселок Рапполово), которые содержались в одинаковых условиях вивария с доступом к воде и корму ad libitum, с 12-часовым режимом освещения. Исследование проведено на модели раневого процесса - плоскостной асептической раны, полученной по методике Д.В. Королева [4]. Животные выводились из эксперимента на 7-е сутки путем применения диэтилового эфира в летальных дозах.
Лабораторные животные были разделены на 5 групп (табл. 2).
Таблица 2. Характеристика групп лабораторных животных

Материал от лабораторных животных фиксировали в растворе нейтрального формалина, заливали в парафин и готовили срезы толщиной 4 мкм. Гистологические препараты были исследованы иммуногистохимическим методом. В качестве маркера был использованы мышиные моноклональные антитела к антигену Ki67. Степень экспрессии Ki67 была выражена количественно на 100 клеток, попадающих в поле зрения при увеличении х1000.
Тип распределения данных определяли по критерию Шапиро-Уилка. Поскольку распределение данных статистически значимо отличалось от нормального, то для их описания использовались медиана (Ме), процентили (Р25-75). Для проверки нулевых гипотез применялся непараметрический критерий Манна-Уитни. Статистически значимыми считали значения р<0,05. Статистический анализ данных выполнен с использованием программного обеспечения STATA 12.1.
Результаты исследования. В результате проведения обзорной флуоресцентной микроскопии было обнаружено свечение в зеленом спектре в гистопрепаратах, как у крыс с раневым дефектом, так и у животных без повреждения кожного покрова (рис. 1).
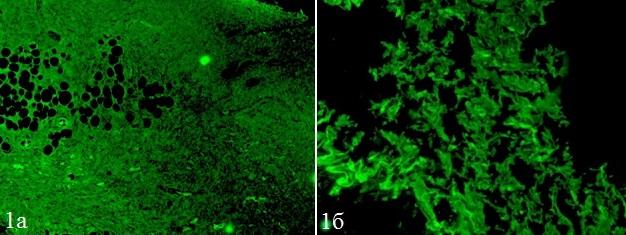
Рис. 1. Картина флуоресцентной микроскопии у животных, на которых был смоделирован раневой процесс (а) и у крыс с неповрежденной кожей (б) (×400).
После ориентировочной флуоресцентной микроскопии (позволившей судить о накоплении исследуемого вещества в тканях лабораторных животных) гистопрепараты были окрашены гематоксилин-эозином (рис. 2, 3).
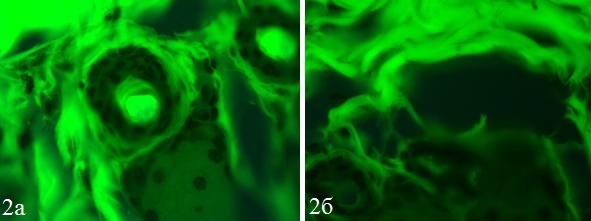
Рис. 2. Картина флуоресцентной микроскопии просветов сосудов и близлежащих клеток у крыс с раневым дефектом (а) и неповрежденной кожей (б). ×400.
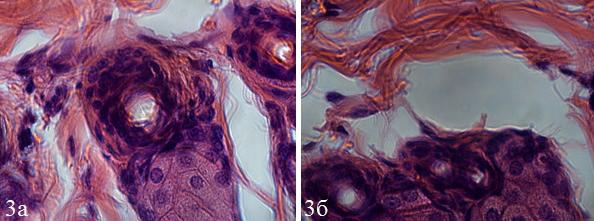
Рис. 3. Окрашивание гематоксилином и эозином просветов сосудов и близлежащих клеток у крыс с раневым дефектом (а) и неповрежденной кожей (б). ×400.
Данные, полученные в ходе изучения фармакокинетических свойств деструктурированный альгиновой кислоты, меченой флуоресцентной меткой, позволяют заключить, что исследуемая оригинальная фармацевтическая субстанция на основе деструктурированной альгиновой кислоты кумулируется в тканях лабораторных животных, как у крыс имеющих раневой дефект, так и животных получавших вещество через неповрежденный кожный покров. Выяснено, что исследуемая субстанция накапливается в области сосудов, окрашивая при этом фибробласты и фиброциты. А также выявлено окрашивание коллагеновых волокон в образцах неповрежденной кожи. Из чего следует, что репаративная активность оригинальной субстанции, вероятно, реализуется за счет влияния на процесс образования коллагена клетками соединительной ткани.
В ходе проведения иммуногистохимического исследования было установлено, что деструктурированный альгинат оказывает влияние на пролиферативную активность клеток (рис. 4), т.к. были выявлены статистически значимые в количестве клеток находящихся в фазах G1, S, G2 и во время митоза, поскольку маркер Кi67 не окрашивает клетки находящиеся в интерфазе (G0), поскольку подвергается катаболизму [3].
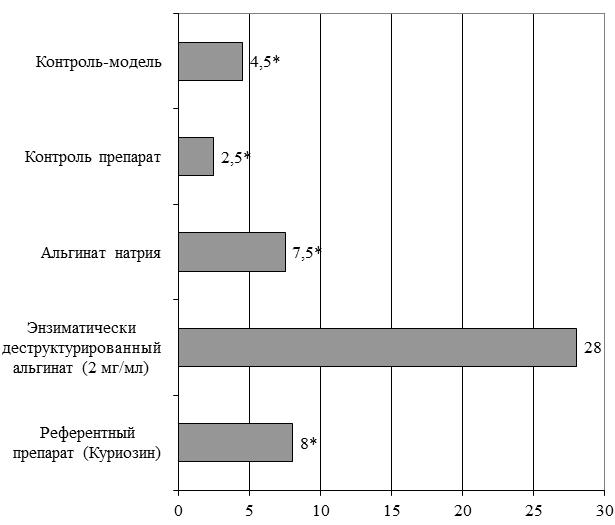
Рис. 4. Результаты иммуногистохимического исследования пролиферативной активности на модели плоскостной асептической раны (маркер пролиферации Ki67, 7-е сутки эксперимента): * - статистически значимые различия при сравнении групп лабораторных животных с группой деструктурированного альгината (р<0,05).
Высокая пролиферативная активность деструктурированной молекулы альгиновой кислоты, с определенной долей вероятности, может быть объяснена, низкой степенью полимеризации и меньшей молекулярной массой по сравнению с нативной молекулой альгината и гиалуроната, а также выявленной способностью кумулироваться в тканях и, возможно, участвовать в биохимических процессах.
Поскольку одна из двух органических кислот образующих альгиновую L-гулуроновая кислота [9] является пространственным изомером D-глюкуроновой кислоты - составной частью химической структуры гликозаминогликанов, участвующих в регуляции многих процессов жизнедеятельности клеток, включая пролиферативную активность [5], то, вероятно, фармакологическая активность деструктурированной альгиновой кислоты объясняется ее высокой биологической доступностью. Между тем, гликозаминогликаны синтезируются фибробластами, накопление в которых деструктурированного альгината «меченного» флуоресцентной меткой и было выявлено.
Выводы. Из вышеописанного можно заключить, что деструктурированная альгиновая кислота способна накапливаться в тканях, как при раневом процессе, так и при отсутствии дефекта кожного покрова. Избирательно кумулироваться в фибробластах, влияя за счет наличия в химическом составе L-гулуроновой кислоты на процесс синтеза гликозаминогликанов, что ведет к повышению пролиферативной активности клеток.
