Согласно оценкам ВОЗ, число заболевших ТБ в 2013 г. составило 9,0 млн. человек, включая более полумиллиона случаев с множественной лекарственной устойчивостью (далее – МЛУ), и 1,5 миллиона человек умирают от этого заболевания [1]. Казахстан относится к 18 странам Европейского региона ВОЗ с высоким уровнем распространения туберкулеза с множественной лекарственной устойчивостью (далее – МЛУ ТБ). Доля новых случаев МЛУ ТБ в 2013 г. составила 3,5% [1]. По итогам 2013 г. уровень первичного МЛУ ТБ по республике составил 25,2%, а приобретенный – 48,6% (в 2012 году, соответственно – 20,8% и 53,3%) [2]. Заболеваемость МЛУ ТБ выросла на 9,3% и составила 11,8 на 100000 населения, против 10,7 за 2012 г. [2]. Из общего числа умерших больных от туберкулеза – 63,5% МЛУ ТБ с БК+ и 23,1% - МЛУ ТБ с БК- [2].
По данным ВОЗ в 2013 г. показатель успешного лечения сохранялся на высоком уровне 86% среди всех новых случаев ТБ, а эффективность терапии противотуберкулезными препаратами второго ряда (далее – ПВР) оставалась относительно низкой, сохраняясь на уровне 48% [1]. К сожалению, в Казахстане излечиваемость новых случаев легочного ТБ с бактериовыделением в 2013 году была значительно ниже и составила 58,0%, МЛУ ТБ – 74,3% [2].
Для лечения ТБ в Научном центре противоинфекционных препаратов (г. Алматы, Казахстан) разработано лекарственное средство – ФС-1, который представляет собой ионный наноструктурированный комплекс из карбогидратов, белков и полипептидов, йода и галогенидов щелочных и щелочноземельных элементов [3, 4].
На основании данных рентгеноструктурного анализа и квантово-химических расчетов предложена модель активного центра препарата ФС-1 [5]. Молекулярный йод находится внутри декстриновой спирали и координируется галогенидом лития и полипептидом, расположенным вне декстриновой спирали (рис.1).
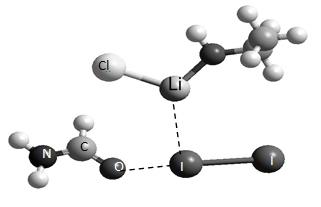
Рис. 1. Структура комплексов йода в препарате ФС-1.
Электронная структура молекулярного йода в препарате ФС-1 отличается от электронной структуры свободного йода и йода в комплексе с биоорганическими лигандами. В активном комплексе этих препаратов молекулярный йод проявляет акцепторные свойства по отношению к полипептидам и донорные по отношению к иону калия. Возможно, эта особая электронная структура йода, не встречающаяся в других лекарственных препаратах, содержащих молекулярный йод, которая обуславливает низкую токсичность препарата.
В межклеточном пространстве под воздействием активного центра препарата структура вирусных или бактериальных ДНК изменяется, более π-донорноактивные, чем белки или пептиды, нуклеотиды патогенной ДНК образуют стабильный комплекс с молекулярным йодом.
Интерпретация данных УФ-спектров водного раствора препарата ФС-1 нуклеотидного триплета (аденозин-гуанозин-аденозин) квантово-химическим методом DFT/B3PW91, свидетельствует о том, что нуклеотиды бактериальной ДНК связываются с молекулярным йодом, координированным галогенидами лития [6].
В настоящее время проведены основные доклинические испытания [7-17], в том числе изучалась in vivo терапевтическая эффективность ФС-1 в различных дозах при МЛУ ТБ и in vitro в различных концентрациях по отношению, как к чувствительному музейному штамму Mycobacterium tuberculosis Н37Rv, так и к резистентным клиническим изолятам. В этих работах была доказана бактерицидная активность ФС-1 по отношению к чувствительному музейному штамму Mycobacterium tuberculosis Н37Rv и к резистентным клиническим изолятам [16]. В экспериментах in vivo доказана терапевтическая эффективность ФС-1 в дозах 2,5 и 4,0 мг/кг в комплексном применении с противотуберкулезными препаратами второго ряда (далее – ПВР), когда наблюдалось 100% абациллирование морских свинок, зараженных МЛУ ТБ, после 60 дней терапии [17]. При комплексном применении препарата ФС-1 с изониазидом у морских свинок, зараженных МЛУ ТБ, был отмечен синергетический эффект, который отразился на повышении противовоспалительного эффекта, на таких клинических проявлениях как восстановление легочной ткани, ее воздушности, на гистологическом восстановлении структуры печени, селезенки [16, 17].
Результаты микробиологических исследований мокроты пациентов туберкулезом легких с множественной лекарственной устойчивостью подтвердили, что применение ФС-1 в комплексе с противотуберкулезными препаратами второго ряда (далее – ПВР) способствовали не только быстрому, но и стойкому абациллированию мокроты с последующим 100,0% излечением пациентов [18].
Одним из основных показателей эффективности противотуберкулезной терапии является прибавка массы тела пациентов, поэтому целью нашего исследования явилось: изучить влияние казахстанского препарата ФС-1 в комплексной противотуберкулезной терапии на массу тела пациентов с МЛУ ТБ.
Материалы и методы
Дизайн исследования: рандомизированное, плацебоконтролируемое, многоцентровое исследование.
Субъекты исследования: пациенты с МЛУ ТБ, подтвержденные культурально, ТЛЧ, и/или бактериоскопически (БК+), (n= 220).
Объект исследования: ФС-1.
Схема исследования:
Для изучения влияния ФС-1 в комплексной противотуберкулезной терапии при МЛУ ТБ были исследованы следующие дозы: 2,0 – 2,5 – 3,0 – 4,0 – 5,0 мг/кг.
Субъекты исследования были рандомизированы на 5 основных и 1 контрольную группы. В основных группах добровольцы получали ПВР + ФС-1; в контрольной группе: ПВР + плацебо. Основные группы были рандомизированы по исследуемым дозам ФС-1: 1 группа – ПВР + ФС-1 2,0 мг/кг; 2 группа – ПВР+ ФС-1 2,5 мг/кг; 3 группа – ПВР + ФС-1 3,0 мг/кг; 4 группа – ПВР + ФС-1 4,0 мг/кг и 5 группа – ПВР + ФС-1 5,0 мг/кг. Продолжительность комплексной терапии составила 6 месяцев. Исследуемый препарат и плацебо принимали 1 раз в сутки, утром, натощак.
Методы исследования
- Ежемесячно пациентов взвешивали утром, натощак, до начала исследования и в течение всего периода лечения, то есть 6 месяцев.
- Бактериологический посев мокроты на микобактерии туберкулеза (2 порции) на среду Ливенштейна-Йенсена осуществляли до начала исследования, каждые 2 недели до 3-х месяцев терапии, далее ежемесячно до 6 месяцев терапии и через 1 год после окончания терапии с применением ФС-1 или плацебо.
- Тест на лекарственную чувствительность к противотуберкулезным препаратам 1, 2 ряда (2 порции) на жидкой и плотной средах.
- Микроскопия мазка мокроты субъектов исследования.
Результаты исследования
Одним из основных показателей положительной клинической динамики при туберкулезной инфекции является повышение массы тела больных. При изучении влияния ФС-1 на массу тела субъектов исследования проводилось сравнение исходного значения с ежемесячными показателями, а также сравнение динамики изменения массы тела субъектов исследования между основными и контрольной группами.
Распределение испытуемых по полу, возрасту и клиническим формам заболевания в группах было однородным, достоверных различий не обнаружено.
Данные по динамике массы тела представлены в табл. 1. Хотя сравнение количественных показателей данных массы тела между группами не выявило достоверных различий в течение всего периода терапии, из таблицы 2 качественные показатели прибавки массы тела, свидетельствовали, что в 1-й группе почти у всех пациентов наблюдалась прибавка в массе тела (94,7%), за исключением 6 месяца терапии (84,2%), (2 – не подъехали на взвешивание), что имело достоверные различия с контрольной группой в течение всего периода терапии: через 3, 4 месяца терапии значение χ2 составило 7,75 (p<0,025); 5 месяцев – 7,94 (p<0,025) и 6 месяцев – 7,75 (p<0,025). Несмотря на то, что во второй группе в 83,3% случаев наблюдалась прибавка массы тела у пациентов в течение всего периода наблюдения, статистический анализ качественных показателей выявил достоверные различия вышеуказанной группы с группой плацебо только через 6 месяцев терапии (p<0,05).
Таблица 1. Сравнительная динамика массы тела в группах, кг (M±m)
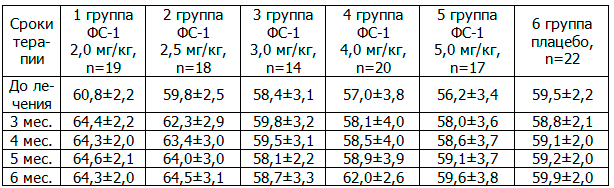
Хотя сравнение количественных показателей данных массы тела между группами не выявило достоверных различий в течение всего периода терапии, из табл. 2 видно, что качественные показатели прибавки массы тела, свидетельствовали о том, что в 1-й группе почти у всех пациентов наблюдалась прибавка в массе тела (94,7%), за исключением 6 месяца терапии (84,2%, 2 – не подъехали на взвешивание), где были выявлены достоверные различия по критерию χ2 с контрольной группой в течение всего периода терапии: через 3, 4 месяца терапии p<0,005; 5, 6 месяцев – p<0,025. Несмотря на то, что во второй группе в 83,3% случаев наблюдалась прибавка массы тела у пациентов в течение всего периода наблюдения, статистический анализ качественных показателей выявил достоверные различия вышеуказанной группы с группой плацебо только через 6 месяцев терапии (p<0,05).
Таблица 2. Качественные показатели динамики массы тела в группах, абс
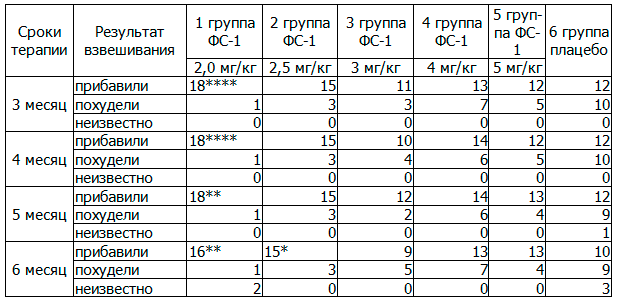
Примечание: * ̶ p<0,05; ** ̶ p<0,025; *** ̶ p<0,01; **** ̶ p<0,005, статистически значимые различия по критерию χ2 между качественными показателями прибавки массы тела в основных группах и контрольной.
Несмотря на то, что при статистическом анализе качественных показателей прибавки массы тела пациентов между остальными основными группами и контрольной достоверных различий не обнаружено, из таблицы 2 видно, что у большинства пациентов остальных основных групп наблюдалась прибавка массы тела, удельный вес которых колебался в пределах 64 до 85,7%. В группе контроля (плацебо) только в 54,5% случаев наблюдалась прибавка массы тела, почти половина пациентов этой группы похудели. К концу терапии удельный вес пациентов контрольной группы, прибавивших в весе снизилось до 45,5%,
В табл. 3 представлены средние значения прибавки массы тела пациентов. Учитывая, что не у вех пациентов наблюдалась прибавка массы тела, и число менялось в течение 6 месяцев, в таблице 3 число пациентов не представлено. Хотя статистический анализ не выявил достоверных различий между основными группами и контрольной, из таблицы видно, что прибавка массы тела в группе плацебо в сравнении с таковыми в основных группах отстает, особенно через 3 и 6 месяцев терапии.
Таблица 3. Сравнительная динамика прибавки массы тела пациентов, кг (M±m)
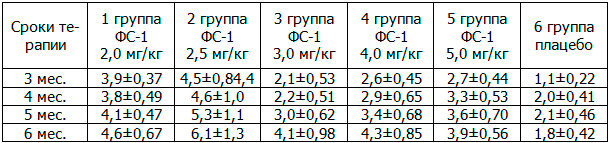
Таким образом, данные исследования показали, что казахстанский препарат ФС-1 при применении в комплексе с противотуберкулезными препаратами второго ряда положительно влиял на один из второстепенных показателей эффективности противотуберкулезной терапии, как прибавка массы тела, которая является одним из признаков восстановления организма и последующего выздоровления. Наиболее эффективной оказалась доза ФС-1 2,0 мг/кг массы тела.
