Современные представления о патогенезе и факторах быстрого прогрессирования остеоартроза (ОА) позволили акцентировать внимание на необходимости назначения больным ОА симптоматических препаратов медленного действия (SYSADOA), из которых первостепенное значение имеют естественные компоненты хрящевого межклеточного вещества – хондроитин сульфат (ХС) и глюкозамин. По рекомендациям EULAR и OARSI они имеют высокий уровень доказательности 1А–1В, что позволяет широко применять эти препараты в клинической практике [5,6,10]. Симптоматическая эффективность и безопасность ХС продемонстрирована во многих клинических и экспериментальных исследования, однако, их результаты очень вариабельны [1,3-4,7-9,11]. Немногочисленны исследования по сравнительной оценке его клинической эффективности при лечении больных гонартрозом и коксартрозом, поэтому данный вопрос является актуальным.
Цель исследования: оценить в сравнительном аспекте эффективность курсового лечения с использованием хондроитина сульфата (ХС) у больных гонартрозом (ГА) и коксартрозом (КА).
Материалы и методы. В исследование было включено 60 амбулаторных больных в состоянии обострения ОА коленных (n=40) и тазобедренных суставов (n=20), соответствующих диагностическим критериям Американской коллегии ревматологов (R. Altman, 1991) [2]. Соотношение женщин и мужчин было 9:1. Средний возраст пациентов составил 56,5 (52; 59,5) лет. Средняя продолжительность заболевания - 6,5 (3,5; 10,5) года. Средняя длительность обострения - 2,5 (1,5; 3,5) месяца. Преобладала II рентгенологическая стадия по классификации Kellgren-Lawrence у 32 (53,3%), реже диагностировали I стадию у 17 (28,3%) и III – у 11 (18,4%) больных. По данным ультразвукового исследования суставов преобладало сочетание признаков синовита и тендинита у большинства пациентов (63,3%).
В зависимости от локализации ОА все больные были разделены на 2 группы: 1 группу составили пациенты с ГА, 2 группу - с КА. Больные обеих групп были сопоставимы по клиническим показателям. Все пациенты получали нестероидный противовоспалительный препарат (НПВП) (найз) по 200 мг/сут в течение 14 дней, а затем по 2 курса 3-х месячной терапии ХС (структум) по 1000 мг/сут с 3-х месячными перерывами. Критериями исключения были ОА IV стадии, посттравматический ОА, артриты другой этиологии, сахарный диабет, тяжелые сопутствующие заболевания внутренних органов, онкологический анамнез.
Динамическое наблюдение выполняли через 1, 3, 6, 9 и 12 месяцев от начала терапии хондропротекторами по основным критериям эффективности: изменение интенсивности болевого синдрома при ходьбе и в покое по ВАШ, динамика функциональных индексов Лекена, WOMAC и суточной потребности в НПВП. Качество жизни больных оценивали по анкете EuroQol-5D (EQ-5D). Дополнительно проводили рентгенологическое и ультразвуковое исследование (УЗИ) пораженных суставов. Протокол исследования был одобрен локальным этическим комитетом. Все пациенты подписали информированное согласие на участие в исследовании. Статистическая обработка полученных результатов была выполнена с использованием программ Excel, Statistica 6.0. Значения переменных представлены в виде медианы с указанием квартилей Ме (Q25; Q75). Для анализа данных применяли метод описательной статистики, для сравнения групп - критерии Манна - Уитни и Вилкоксона. Результаты считали достоверными при уровне значимости р < 0,05.
Результаты и обсуждение. Клиническая характеристика больных ОА, разделенных на группы ГА и КА, представлена в табл. 1.
Таблица 1. Клиническая характеристика больных ОА
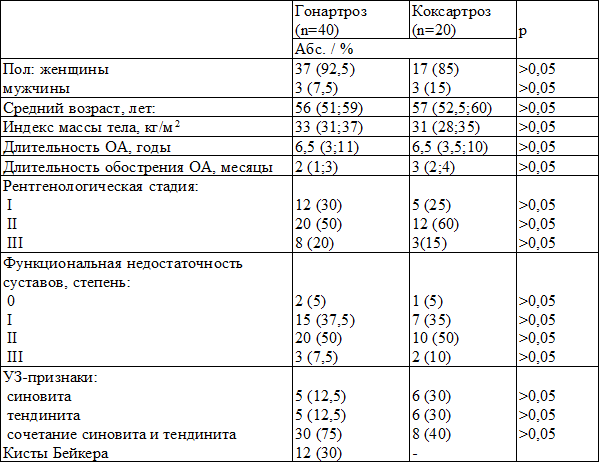
Из представленных данных следует, что обе группы были сопоставимы по всем клиническим параметрам: возрастно-половому составу, продолжительности ОА и длительности обострения, рентгенологической стадии, степени функциональной недостаточности суставов и ИМТ.
Таблица 2. Клинические показатели и параметры качества жизни до начала лечения и их динамика
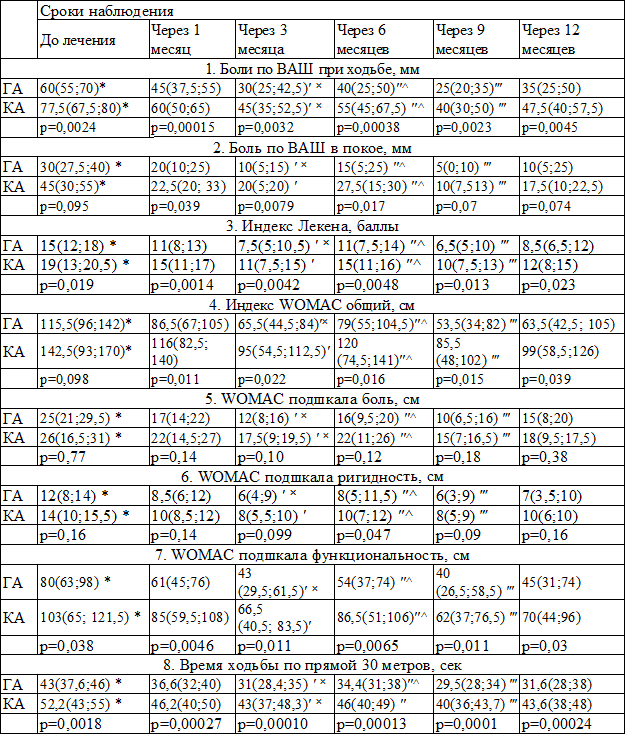
Примечания: U-test-MW-р - значение статистических различий между подгруппами ГА и КА (критерий Манна-Уитни); статистически значимые различия между показателями разных сроков наблюдения внутри подгрупп ГА и КА (критерий Вилкоксона): *р < 0,05 – до лечения и 1, 3, 6, 9, 12 месяцами; ′р < 0,05 – между 3 и 6 месяцами; ˟ р < 0,05 – между 3 и 9 месяцами; ″р < 0,05 – между 6 и 9 месяцами; ^р < 0,05 – между 6 и 12 месяцами; ‴р < 0,05 – между 9 и 12 месяцами
Исходные клинические показатели и параметры качества жизни до начала лечения и их динамика на фоне курсовой терапии структумом представлены в табл. 2. Тяжесть клинического состояния у больных ОА до начала лечения зависела от локализации процесса. При анализе исходных показателей выраженности болевого синдрома и функциональной недостаточности суставов по соответствующим шкалам и индексам обнаружены наиболее худшие их значения у больных КА, причем, статистически значимыми различия были в отношении боли при ходьбе по ВАШ, функционального индекса Лекена, подшкалы «функциональность» индекса WOMAC, теста ходьбы по прямой. Таким образом, при КА определялись более выраженная интенсивность болевого синдрома и ограничения функционального статуса больных.
Наличие боли и функциональных ограничений в суставах негативно отразились на параметрах КЖ больных ОА. Так, характеристика больных ГА и КА по 5 категориям анкеты EQ-5D (проблемы с передвижением в пространстве, самообслуживанием, повседневной деятельностью, наличием боли и/или дискомфорта и чувства тревоги/депрессии) показала снижение параметров КЖ по всем 5 категориям, причем, наиболее значимыми были изменения в отношении боли и/или дискомфорта (средний балл при ГА составил 2,86, при КА – 2,95), передвижения (2,28 и 2,55), повседневной активности (2,33 и 2,6). Проведенное сравнение КЖ в зависимости от поражения коленных или тазобедренных суставов выявило, что ухудшение состояния здоровья за последний год отмечало подавляющее большинство больных ОА (80% - ГА, 85% - КА), но у больных КА определялись статистически значимо более выраженные проблемы с передвижением, самообслуживанием, повседневной активностью. К проблемам, связанным с физическим функционированием, присоединяются нарушения психологического характера у больных ГА и КА, однако, при КА большее количество пациентов испытывают выраженное чувство тревоги/депрессии (70%). Показатели общего состояния здоровья по «термометру здоровья» EQ-5D отличались от популяционной нормы (82 мм) и также были достоверно хуже при КА, чем при ГА (22,5 (15; 35) мм против 40 (30; 50) мм, р=0,002). Индекс EQ-5D при КА составил 0,0055 (-0,074; 0,289) и был значимо хуже, по сравнению с ГА - 0,354 (0,108; 0,421) (р<0,05) при средних популяционных значениях (0,86±0,23). Таким образом, при КА отмечалось более значительное ухудшение параметров КЖ, по сравнению с ГА.
Проведен анализ динамики клинических показателей и параметров КЖ в зависимости от локализации ОА у больных, получавших курсовое лечение с использованием структума в течение 12 месячного наблюдения (табл. 2).
В течение 12 месячного наблюдения у больных ГА и КА отмечалось волнообразное течение симптоматики ОА с периодами улучшения на фоне лечения и последующего ухудшения клинических показателей в отсутствии приема структума. При этом выявлены различия в выраженности симптоматической эффективности и длительности последействия структума в зависимости от локализации ОА. Начиная уже с 1 месяца от начала сочетанного лечения с использованием структума и найза все клинические показатели были статистически значимо лучше исходных и различия сохранялись на протяжении всего срока наблюдения. Причем, положительная динамика в течение 1 месяца была более выраженная у больных ГА, чем КА особенно в отношении общего индекса WOMAC и подшкалы «боль», «функциональность».
Через 3 месяца от начала лечения сохранялась тенденция более выраженной динамики клинических показателей при ГА, чем при КА. Так, боли при ходьбе и в покое по ВАШ уменьшились при ГА на 50% и 83%, при КА на 48% и 66%. Значения индекса Лекена сократились на 53% при ГА и 48% при КА. Значения общего индекса WOMAC и его подшкал «боль», «скованность», «функциональность» больше уменьшились при ГА – на 49%, 61%, 56%, 49%, чем при КА – на 37%, 36%, 49%, 40%. Сохранились различия между группами по всем показателям, кроме подшкалы «боль» и «скованность» индекса WOMAC.
Через 6 месяцев от начала наблюдения у больных как ГА, так и КА определялось ухудшение клинических показателей и средние их значения стали достоверно хуже по сравнению с предыдущим сроком. После 2 курса терапии структумом (через 9 месяцев от начала наблюдения) также был достигнут достоверный положительный симптоматический эффект в обеих группах по сравнению с предыдущим сроком наблюдения, который был статистически значимо более выраженным по всем клиническим показателям у больных ГА. У больных КА эффект был только в отношении боли по ВАШ при ходьбе и подшкалы «боль» индекса WOMAC. Достигнутые значения на этом сроке были статистически значимо лучше по большинству показателей по сравнению с 1 курсом терапии. Очередной 3-хмесячный перерыв в лечении (через 12 месяцев от начала наблюдения) привел к статистически значимому ухудшению всех клинических показателей в обеих группах по сравнению с предыдущим сроком наблюдения. Тем не менее, достигнутые значения оставались достоверно лучше исходных и значений перед началом 2 курса терапии у больных обеих локализаций ОА.
В течение 12 месяцев наблюдения также отмечалась волнообразная динамика изменения параметров КЖ по анкете EQ-5D. Так, после 2-х курсов терапии структумом значения по всем категориям значимо улучшились, оценка общего состояния здоровья по «термометру здоровья» повысилась и почти достигла уровня популяционной нормы только у больных ГА (80(67,5;85) мм), а при КА составила 65 (50; 72,5) мм. Был рассчитан индекс EQ-5D на разных сроках наблюдения и его значения представлены на рис. 1. Из продемонстированных данных следует, что значения индекса EQ-5D статистически значимо улучшились после 1 курса терапии как при ГА, так и при КА. После 2 курса терапии наиболее стремительное повышение значения индекса отмечено при КА, однако, ближе к популяционной норме его значения приблизились у больных ГА. Через 6 и 12 месяцев от начала лечения все параметры КЖ несколько ухудшились, но оставались статистически значимо лучше исходных значений. Динамика клинических показателей подтверждалась данными УЗИ суставов (рис. 2).
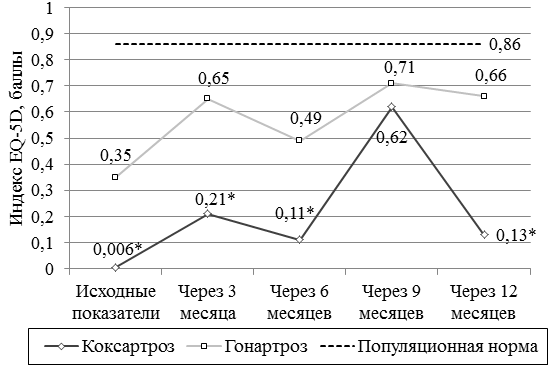
Рис. 1. Динамика значений индекса EQ-5D у больных ГА и КА на фоне лечения структумом: *р < 0,05 – статистически значимые различия между группами ГА и КА
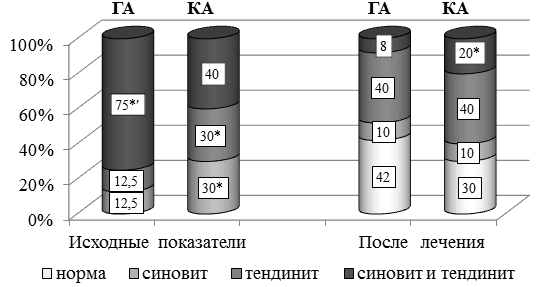
Рис. 2. Динамика частоты выявления УЗ-признаков синовита и тендинита у больных ГА и КА до и после лечения структумом (%): *р < 0,05 – статистически значимые различия между группами ГА и КА; ʹр < 0,05 – статистически значимые различия внутри групп ГА и КА (критерий Манна-Уитни)
Из рис. 2 следует, что по итогам 2-х курсов терапии выявлена положительная динамика по данным УЗИ суставов у пациентов обеих локализаций ОА. У 42% больных ГА наблюдалась нормализация УЗ параметров. У 58% сохранялись УЗ признаки воспалительного процесса, причем, преобладали признаки тендинита у 40% больных, а сочетание синовита и тендинита отмечалось только у 8% пациентов. У больных КА нормализация УЗ параметров была в 30%, у 70% сохранялись признаки воспалительных проявлений, причем, у 40% - тендинит и у 20% - сочетание бурсита и тендинита. Следовательно, при ГА также отмечалась более выраженная положительная динамика данных УЗИ суставов, чем при КА. Эффективность проводимой терапии подтверждалась динамикой снижения потребности в приеме НПВП (табл. 3).
Таблица 3. Динамика потребности в приеме найза у больных ГА и КА
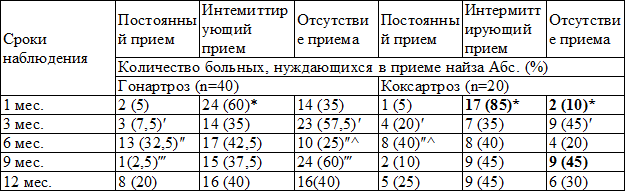
Примечания: U-test-MW-р - значение статистических различий между подгруппами ГА и КА (критерий Манна-Уитни); статистически значимые различия между показателями разных сроков наблюдения внутри подгрупп ГА и КА (критерий Вилкоксона): *р < 0,05 – до лечения и 1, 3, 6, 9, 12 месяцами; ′р < 0,05 – между 3 и 6 месяцами; ˟ р < 0,05 – между 3 и 9 месяцами; ″р < 0,05 – между 6 и 9 месяцами; ^р < 0,05 – между 6 и 12 месяцами; ‴р < 0,05 – между 9 и 12 месяцами
Из табл. 3 видно, что по окончании как 1, так и 2 курса терапии с использованием структума отказалось от приема НПВП около 60 % больных ГА и меньшее количество больных КА (45%). Перед началом 2 курса лечения только по 20% больных ГА и КА не принимали НПВП. Через 12 месяцев от начала наблюдения потребность в приеме НПВП опять увеличилась, но была несколько ниже, чем через 6 месяцев от начала терапии, а в приеме НПВП не нуждались 40 % больных ГА и 30 % больных КА.
Выводы
1. По результатам проведенного годичного курсового лечения с использованием хондроитина сульфата у больных остеоартрозом наилучшая эффективность была получена при гонартрозе, по сравнению с коксарторозом.
2. При коксартрозе отмечалась по клиническим показателям и параметрам качества жизни более выраженная тяжесть процесса.
3. Эффект последействия препарата сохранялся не более 3-х месяцев после каждого курса терапии у больных как гонартрозом, так и коксартрозом.
