Грыжи передней брюшной стенки остаются одной из самых распространенных хирургических патологий. Проблема хирургического лечения больных с ущемленными вентральными грыжами на сегодняшний день остается актуальной, требует дополнительного изучения и разработки стандартов оказания квалифицированной помощи. Заболеваемость населения составляет 4-7%, а у лиц пожилого и старческого возрастов достигает 15-17% [1, 3, 4,].
В структуре пациентов поступающих в хирургические отделения стационаров по экстренным показаниям, ущемленные грыжи занимают четвертое место, уступая острому панкреатиту, острому аппендициту и острому холециститу, а среди неотложных вмешательств занимают третье место после аппендэктомии и холецистэктомии. Ущемление развивается у 8-20% больных с наружными грыжами брюшной стенки [7,9].
Потребность в оперативном лечении составляет около 8 - 10% от всех хирургических вмешательств, причем неуклонно растет удельный вес больных с ущемленными послеоперационными вентральными грыжами (ПОВГ) [2]. Частота рецидива ПОВГ после различных способов пластик передней брюшной стенки находится в очень широком диапазоне: от 3,9% до 70% [6, 10].
Несмотря на множество предложенных способов герниопластики, результаты лечения ущемленных грыж передней брюшной стенки часто не удовлетворяют ни пациентов, ни хирургов [8]. По-прежнему на достаточно высоком уровне сохраняются: низкая эффективность многочисленных аутопластических методов, используемых при грыжесечениях, частая инвалидизация больных, высокий процент рецидивов и развития осложнений среди оперированных пациентов, частота летальных исходов.
Таким образом, проблема хирургического лечения ущемленных грыж передней брюшной стенки в настоящее время до конца не решена, требует выработки более четкого и систематизируемого протокола ведения таких пациентов, накопления и анализа имеющегося материала и дальнейшего уточнения [5, 11].
Цель исследования - улучшение результатов хирургического лечения и профилактики раневых осложнений у больных с ущемленными грыжами передней брюшной стенки, путем использования синтетических эндопротезов, воздействия низкоинтенсивного лазерного излучения и применения компьютерной термографии, как метода диагностики послеоперационных осложнений.
Материалы и методы исследования. Материалом настоящей работы являются результаты ретроспективного и проспективного исследования 265 больных с ущемленными паховыми, пупочными и послеоперационными вентральными грыжами, которые находились на лечении в клинике госпитальной хирургии ГБОУ ВПО «Самарский государственный медицинский университет» с 2006 по 2012 г. включительно.
В зависимости от способа пластики, использования низкоинтенсивного лазерного излучения (НИЛИ) в интра – и послеоперационном периодах и компьютерной термографии, больные с ущемленными грыжами были разделены на две группы: основную и контрольную, которые в свою очередь подразделялись на основную группу I, II и контрольную группу I,II. Данные представлены в табл. 1.
Основную группу I составили 68 больных, оперированных без предварительного отбора по поводу ущемленной вентральной грыжи различной локализации ненатяжными способами пластики с использованием сетчатого протеза, НИЛИ и компьютерной термографии в послеоперационном периоде.
Таблица 1. Распределение больных по группам

Вторую основную группу составили 70 пациентов с ущемленными грыжами, оперированных с применением традиционных методов герниопластики, использованием НИЛИ и компьютерной термографии в послеоперационном периоде.
Контрольную группу I составили 67 больных, оперерованных ненатяжными способами пластики с использованием сетчатого протеза, но без применения НИЛИ и компьютерной термографии в послеоперационном периоде.
Вторую контрольную группу составили 60 больных, оперированных с применением традиционных способов аутопластики передней брюшной стенки, без применения НИЛИ и компьютерной термографии в послеоперационном периоде.
Больные основных и контрольных групп по локализации ущемленной грыжи условно разделены на три подгруппы (табл. 2).
Таблица 2. Распределение больных по виду грыжи
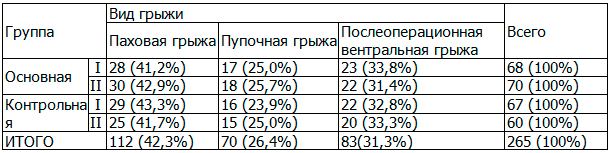
На основании проведенного исследования выявлено, что в основных и контрольных группах преобладают пациенты, оперированные с ущемленной паховой и послеоперационной вентральной грыжами.
Возраст пациентов, оперированных с использованием различных способов пластики и применением НИЛИ, составил от 22 до 82 лет. Средний возраст 58,6±10,4 лет. Из оперированных больных мужчин было – 98 (71,0%), женщин – 40 (29,0%).
Возраст пациентов, оперированых с применением различных способов ненатяжной и натяжной пластики, но без применения НИЛИ составил от 23 до 81 года. Средний возраст 58,1±10,3 лет. Из оперированных пациентов мужчин – 94 (74,0%), женщин – 33 (26,0%).
Статистически значимых различий по полу и возрасту в исследуемых группах не выявлено. Следует отметить, что большая часть пациентов – лица трудоспособного возраста от 40 до 55 лет, что обуславливает большую социальную значимость изучаемой проблемы. У пациентов обеих групп наиболее частыми сопутствующими заболеваниями явились следующие: сахарный диабет (15,9 %), гипертоническая болезнь (21,3 %), ишемическая болезнь сердца (33,5 %) и др.(17,3 %).
По срокам госпитализации от начало ущемления больные основных и контрольных групп распределены следующим образом (табл. 3).
Таблица 3. Распределение больных по срокам госпитализации от начала ущемления грыжи
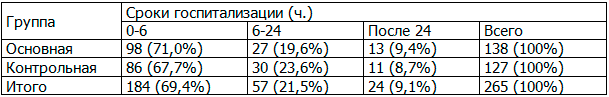
После госпитализации все больные оперированы в течение двух часов.
В результате проведенного исследования необходимо отметить, что характер патологических изменений органов в грыжевом мешке при ущемленной грыжи был неодинаков. Так, в основной группе I, из 68 больных у 27 (39,7%) пациентов ущемленный орган оказался жизнеспособным, а некроз ущемленного органа наблюдался у 41 (60,3%) человек. При этом у 25 (36,8%) больных в грыжевом мешке имелся ущемленный некротизированный сальник и у 16 (23,5%) – некроз участка кишки. Соответственно в 25 случаях была выполнена резекция сальника в пределах жизнеспособных тканей и 16 – резекция тонкой кишки с анастомозом «бок в бок». Надо отметить, что во всех случаях резекция нежизнеспособного органа выполнялась через герниолапаротомию.
В основной группе II, из 70 пациентов жизнеспособный орган оказался у 31 (44,3%) больных, а у 39 (55,7%) наблюдался некроз ущемленного органа, при этом у 26 (37,1%) из них был ущемлен и некротизирован большой сальник, а у 13 (18,6%) – диагностирован некроз ущемленной тонкой кишки. Всем больным с некротизированным в грыжевом мешке органом производилась его резекция.
При исследовании контрольной группы I выявлено, что из 67 больных, жизнеспособный орган оказался у 29 (43,3%) пациентов, тогда как у 38 (56,7%) имелся некроз ущемленного органа, среди которых у 24 (35,8%) был ущемлен и некротизирован большой сальник, а у 14 (20,9%) - некроз участка кишки. Во всех случаях выполнялась резекция нежизнеспособного органа.
Во II контрольной группе ущемленный орган оказался жизнеспособный у 28 (46,7%) из 60 больных, а некроз ущемленного органа отмечался у 32 (53,3%) пациентов. При этом у 17 (28,3%) больных в грыжевом мешке имелся ущемленный и некротизированный сальник и у 15 -(25,0) диагностирован некроз ущемленной тонкой кишки. Как и в предыдущих случаях, всем больным с некротизированным в грыжевом мешке органом выполнялась его резекция.
Больным II основной и II контрольной групп, при хирургическом лечении ущемленных грыж без использования сетчатого эндопротеза, выполнялось грыжесечение с традиционной пластикой.
Так, при лечении ущемленных паховых грыж предпочтение отдавали методам пластики по Bassini, Postempski, Жирару – Спасокукоцкому со швами Кимбаровского, при ущемленных пупочных грыжах применялись способы Мейо и Сапежко, а при ущемленной ПОВГ – пластика дефекта апоневроза по Сапежко.
Из 135 операций 17 (12,6%) выполнены с использованием полипропиленового сетчатого протеза «PROLENE» производства «Ethicon, Johnson & Johnson», а в 118 (87,4%) случаях применялся полипропиленовый сетчатый протез АОЗТ СП «Линтекс-эсфил» (г. Санкт-Петербург). Эксплантат фиксировался полипропиленовой нитью № 2/0. Выбор фирмы, производящей сетчатый протез, случаен. Единственным строгим условием выбора были материал и структура сетчатого протеза - полипропиленовый, макропористый, монофиламентный эксплантат. Показанием для использования полипропиленового сетчатого протеза являлся дефект грыжевых ворот диаметром более 5 см.
При лечении больных I и II основных групп с пупочными грыжами, осложненные некрозом ущемленного органа, большыми послеоперационными вентральными грыжами выполнялась герниолапаротомия с последующей пластикой передней брюшной стенки ненатяжными и традиционными способами. Для этого требовалась довольно обширная отслойка подкожной жировой клетчатки от апоневроза, что в свою очередь приводит к образованию остаточной полости над сетчатым эндопротезом и между апоневрозом и подкожной жировой клетчаткой при натяжных способах пластики, которая вследствие ряда причин может сопровождаться образованием сером, гематом, абсцесса и т.д. в раннем послеоперационном периоде.
Для уменьшения остаточной полости, анатомо-физилогического сопоставления тканей в послеоперационной ране, уменьшения количества раневых послеоперационных осложнений и возможного рецидива грыжеобразования нами предложено и применено у 30 больных основных групп - устройство для профилактики эвентерации (патент РФ на полезную модель № 103462 от 28.04.2010) (рис. 1).
Интраоперационно, местно в зону пластики, а также в послеоперационном периоде больным с ПОВГ, рецидивными паховыми и пупочными грыжами, где проводилось дренирование послеоперационной раны, через дренаж по Редону или чрескожно на область раны проводилось воздействие низкоинтенсивным лазерным излучением с помощью аппарата «Креолка-32» длиной волны 630 нм, мощностью 3мВт/см2 с экспозицией 3-5 мин.
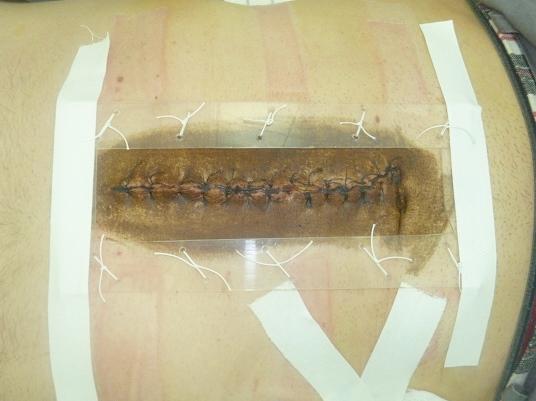
Рис. 1. Использование устройства для профилактики эвентерации
Режим непрерывный. Для этих целей применялся гибкий волокнистый световод. Лазеротерапию проводили ежедневно, начиная со второго дня после операции. Курс лечения зависел от вида пластики, площади сетчатого эндопротеза, течения послеоперационного периода и в среднем составил 6±2 дня. НИЛИ обладает проникающей способностью в ткани, улучшает лимфо- и гемоциркуляцию, что проявляется в уменьшении отделяемого из раны, усилении репаративных процессов и ускорении регенерации тканей в зоне пластики. При этом снижается уровень местных воспалительных реакций, интенсивность болевого синдрома, сроки дренирования и госпитализации.
Всем больным выполнялись общеклинические методы исследования, ультразвуковое исследование брюшной полости и грудной клетки (по показаниям), рентгенография брюшной полости, измерение внутрибрюшного давления, компьюторная термография в послеоперационном периоде, цитологические, социологические и статистические методы исследования.
Результаты исследования и их обсуждение. В послеоперационном периоде в основной группе I (n=68) ранние послеоперационные осложнения наблюдались у 6 (8,9%) больных, в контрольной группе I (n=67) – у 22 (32,8%) пациентов, а в основной группе II (n=70) – у 11 (15,7%) и контрольной группы II (n=60) – у 32 (53,4%) больных соответственно.
У пациентов с пластикой передней брюшной стенки сетчатым эндопротезом I основной и I контрольной групп, чаще всего формировалась серома - в 3 (4,4%) и 10 (14,9%) случаях соответственно. Гематома в области послеоперационной раны выявлена у 1 (1,5%) больного основной группы I и у 3 (4,5%) пациентов I контрольной группы. Инфильтрат послеоперационной раны наблюдался в 2 (3,0%) случаях у больных I основной группы и в 8 (11,9%) случаях I контрольной группы. Кроме того у 1 (1,5%) пациента I контрольной группы отмечалось нагноение послеоперационной раны.
Среди пациентов, оперированных с традиционной пластикой, использованием НИЛИ и устройства для профилактики эвентерации (основная группа II, n=70) раневые послеоперационные осложнения выявлены у 11 (15,7%) больных. Среди них: гематома – у 2 (2,9%), инфильтрат – у 5 (7,1%), серома – у 4 (5,7%) больных.
У пациентов, оперированных с применением натяжных методов пластики, но без использования НИЛИ, устройства для профилактики эвентерации и компьютерной термографии (контрольная группа II, n=60) нагноение послеоперационной раны наблюдалось в 3 (5%) случаях, инфильтрат в 13 (21,7%), гематома в 3 (5%) и серома в 13 (21,7%) случаях.
Нагноение послеоперационной раны наблюдалось - у 1 (1,5%) больного I контрольной и - у 3 (5%) пациентов II контрольной групп, а в I и II основных группах нагноения послеоперационной раны не было. Отторжения сетчатого протеза нами не выявлено.
Таким образом, исследование осложнений раннего послеоперационного периода у больных с ущемленными грыжами передней брюшной стенки, при различных способах пластики показало, что частота их возникновения у пациентов с протезирующими методами пластики, не превышает данную частоту у больных, оперированных традиционными способами пластики. Различия статистически достоверны, р<0,05. Однако отмечается снижение частоты послеоперационных раневых осложнений, таких как: серома и нагноение послеоперационной раны у больных с применением НИЛИ и устройства для профилактики эвентерации, по сравнению с пациентами, которым НИЛИ и данное устройство не применялись.
Данные осложнения легко диагностировались при использовании компьютерной термографии и ультразвукового исследования. Во всех случаях, прогнозируя его, нам удалось справиться с данными осложнениями без каких – либо последствий.
Отдаленные результаты лечения. Нами обследованы 97 (70,3%) из 138 больных основных групп и 89 (70%) из 127 пациентов контрольных групп в сроки от 1 до 6 лет (4,3±1,5 лет). Всего из 265 больных обследовано в отдаленном периоде – 186 (70,2%).
Количество лигатурных абсцессов и свищей послеоперационного рубца у больных с применением сетчатого протеза и НИЛИ выявлено в 1 (2,0%) случае, а без применения НИЛИ – у 5 (10,7%) пациентов, хронический болевой синдром отмечался у 2 (4%) и 6 (12,8%) пациентов I основной и I контрольной групп соответственно. Рецидивов грыж в сроки от 1 до 6 лет в исследуемых группах нами не выявлено.
Из 47 обследованных пациентов, оперированных традиционными способами пластики и использованием НИЛИ, количество рецидивов в сроки от 1 до 6 лет выявлено - в 8 (17%) случаях, лигатурных абсцессов и хронического болевого синдрома в области послеоперационного рубца – в 3 (6,4%) и 1 (2,1%) случаях соответственно, тогда как из 42 обследованных пациентов с применением пластики местными тканями, но без использования НИЛИ и устройства для профилактики эвентерации, рецидив выявлен - у 16 (38,1%) больных, лигатурный абсцесс – у 7 (16,7%), а хронический болевой синдром в зоне операции – у 5 (12%) пациентов.
Самый высокий процент рецидива выявлен у больных контрольной группы II с ПОВГ – 19,0%. Также высокий процент рецидивов выявлен у больных с паховой грыжей – 12 % и пупочной грыжей – 7,1 %.
Воздействие лазерного излучения в послеоперационном периоде способствовало уменьшению болевого синдрома, снижению сроков дренирования (4,2±1,0 день у больных основных групп, 8,1±1,0 дня у групп сравнения, которым НИЛИ не проводилось); снижению процента ранних послеоперационных осложнений, рецидивов ПОВГ и сроков госпитализации. Средний койко-день в основной группах составил: при паховых и пупочных грыжах 6,2±1,0 день, при ПОВГ с применением НИЛИ 11,6±1,0 день, а в группе сравнения 8,4±1,0 день и 17,6±1,0 соответственно.
Для оценки микроциркуляции в зоне оперативного вмешательства использовался компьютерный тепловизор «ИРТИС - 2000». Локальную термометрию выполняли на 3,5 и 7 сутки после оперативного вмешательства всем больным I, II основных групп, при подозрении на воспалительный процесс в зоне пластики. Контролем достоверности полученных результатов явилось «красное тело» с постоянной температурой 33,0ºС.
Анализ полученных результатов исследования позволил нам выявить, что при благоприятном течении послеоперационного периода у всех больных I, II основных групп в первые сутки (1 – 3 сутки) имеется наличие локальной умеренной гипертермии, соответствующий площади сетчатого эндопротеза на величину от 0,2 ºС до 1,6 ºС, что свидетельствует об умеренной воспалительной реакции и хорошей микроциркуляции. На 3-5 сутки повышение местной температурной реакции со стороны оперативного вмешательства колебалось от 0,8 до 1,8ºС, что также может свидетельствовать об асептическом воспалении – естественной реакции на оперативное вмешательство (рис. 2).
На 7-8 сутки термопрофиль зоны операции практически не отличался от окружающих тканей, разница температур составляла 0,2–0,5 ºС.
Установлено, что при повышении локальной температуры у больных в пределах от 0,2 до 1,8ºС отмечается гладкое течение послеоперационном периода и отсутствие осложнений, что наблюдалось в 88,1% случаев у пациентов I основной группы и в 82,9% случаев у больных II основной группы. Повышение локальной температурной реакции в зоне пластики от 1,9 до 2,9 ºС свидетельствовал о наличии инфильтрата или серомы в области послеоперационной раны. При повышении температуры более чем на 3,0 ºС, свидетельствовало о гнойно – септическом воспалении в области послеоперационной раны. Данная ситуация наблюдалась у 1,4% прооперированных больных основных групп.
Все вышеперечисленное позволило нам простым и неинвазивным методом осуществить объективную оценку локального статуса, прогнозировать развитие послеоперационных раневых осложнений и своевременно корректировать хирургическую тактику.
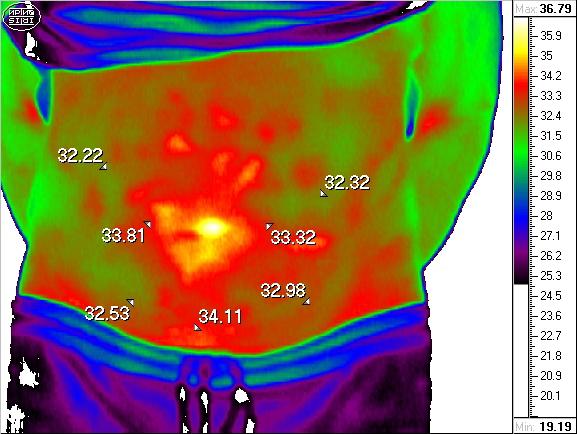
Рис. 2. Термограмма больного М., 62 лет с ущемленной пупочной грыжей (5-е сутки после герниопластики сетчатым протезом «sublay»)
Заключение. Применение нами полипропиленовых макропористых, монофиламентных сетчатых эндопротезов в пластике при ущемленных грыжах под прикрытием антибиотикопрофилактики, антибиотикотерапии, устройства для профилактики эвентерации при ущемленных ПОВГ и воздействия на зону пластики НИЛИ, позволило нам достичь лучших результатов как в раннем, так и в позднем послеоперационных периодах, по сравнению с традиционной пластикой. Так общее количество ранних послеоперационных осложнений в контрольной группе I составило – 32,8%, контрольной группе II – 53,4%, а в основных группах – 8,9% и 15,7% соответственно.
1. Сроки госпитализации больных с пластикой сетчатым протезом, которым проводились сеансы лазеротерапии, использовалось устройство для профилактики эвентерации и компьютерная термография с целью профилактики и программирования раневых осложнений в среднем на 6 – 7 дней ниже, особенно у больных с ПОВГ.
2. Применение протезирующих методов пластики, НИЛИ у больных с ущемленными вентральными грыжами привело к снижению частоты рецидива заболевания практически до нуля. Отторжения сетчатых протезов нами не наблюдалось. Отдаленные результаты лечения больных с ущемленными грыжами, с применением протезирующих методов пластики и предложенными нами способов профилактики раневых осложнений сопоставимы с достигнутыми результатами лечения в плановой хирургии грыж.
3. Общие результаты лечения больных с ущемленными грыжами передней брюшной стенки, оперированных с использованием сетчатого эндопротеза, НИЛИ в интра – и послеоперационных периодах, компьютерной термографии для прогнозирования и профилактики раневых осложнений можно признать хорошими.
Таким образом, протезирующие методы пластики при ущемленных грыжах передней брюшной стенки с применением НИЛИ, компьютерной термографии, в качестве метода для прогнозирования, профилактики раневых осложнений и устройства для профилактики эвентерации, позволяют достоверно улучшить отдаленные результаты хирургического лечения, по сравнению с традиционной пластикой.
