Введение. Одной из самых актуальных проблем в современной хирургии и в частности анестезиологии является проблема развития и профилактики различных послеоперационных осложнений, обусловленных побочным действием анестетиков, используемых в ходе анестезиологического обеспечения. К таким осложнения относят, в первую очередь, синдром послеоперационных когнитивных дисфункций (ПОКД) [1-3] и синдром послеоперационной тошноты и рвоты (ПОТР).
В последнее время в мире специалистами в области анестезиологии и реаниматологии, а так же неврологии уделяется достаточно большое внимание такому явлению как синдром послеоперационной когнитивной дисфункции (ПОКД) [6]. На данный момент во всем мире общепризнанно, что стойкая ПОКД после операций в условиях общей анестезии реальна и намного чаще встречается, чем это было принято считать ранее [4,5,7].
Одно из самых крупных проведенных международных проспективных рандомизированных исследований (International Study of Post-Operative Cognitive Dysfunction 1994-2000), показало, что частота ранней послеоперационной когнитивной дисфункции в хирургической практике составляет минимум 20-30% [3,6]. Таким образом, ПОКД является одним из нежелательных феноменов, связанных с применением общей анестезии. Послеоперационные когнитивные расстройства приводят к удлинению сроков госпитализации, увеличению осложнений и ухудшению качества жизни пациентов. В связи с этим в особенно остро последнее время стали обсуждаться вопросы профилактики послеоперационных когнитивных нарушений.
Наряду с ПОКД проблема послеоперационной тошноты и рвоты также считается одной из важнейших в современной хирургии и анестезиологии [8,9]. По данным статистики, синдром послеоперационной тошноты и рвоты (ПОТР) – самое частое осложнение первых суток после любых хирургических вмешательств, выполненных в условиях как общей, так и регионарной анестезии [8,9,12]. Этот синдром существенно ухудшает течение послеоперационного периода и может стать причиной серьезных осложнений таких как аспирация, развитие электролитных нарушений, нарушение гемодинамики, усиление послеоперационного кровотечения, повышение внутричерепного и внутрибрюшного давления, усиление послеоперационной боли [8,12]. Этиология ПОТР многофакторна: применение ингаляционных анестетиков, стрессовые метаболические нарушения, послеоперационная гипоксия, нарушение гемодинамики и т.д. [13]. Большинство исследователей по всему миру отмечают, что частота ПОТР зависит от множества факторов (возраст, пол, характер оперативного вмешательства, вид анестезиологического обеспечения, послеоперационные факторы) и может колебаться от 20 до 70% [8,10].
Цель исследования. Изучить частоту развития синдрома ПОКД и синдрома ПОТР после планового оперативного лечения переломов проксимального отдела бедренной кости (ППОБК), в раннем и позднем послеоперационном периоде и оценить взаимосвязь уровня тревожности до операции и степень выраженности ПОКД после оперативного лечения в зависимости от вида анестезиологического обеспечения.
Материал и методы. Для решения поставленных задач было обследовано 50 пациентов пожилого и старческого возраста, находившихся на плановом оперативном лечении в травматологическом отделении ГБУЗ Областная клиническая больница Тверской области, которым были выполнены операции тотального протезирования тазобедренного сустава или остеосинтез вертельного перелома.
Критериями включения в исследование являлись:
1. информированное согласие пациентов на участие в исследовании;
2. возраст старше 65 лет,
3. физический статус по ASA II (16%) - ASA III (74%),
4. плановое оперативное лечение
5. продолжительность оперативного вмешательства не менее 60 минут
Критериями исключения являлись:
1. отсутствие информированного согласие пациентов на участие в исследовании;
2. физический статус по ASA IV (плохо контролируемые сопутствующие заболевания с потенциальной угрозой жизни);
3. наличие исходного когнитивного дефицита;
4. продолжительность оперативного вмешательства менее 60 минут.
В зависимости от анестезиологического обеспечения было выделено 2 группы. В первой группе (32 пациента) использовалась общая сбалансированная анестезия на основе севофлурана (2,5 - 3 об. %) и фентанила (3–5 мкг/кг), во второй группе (18 пациентов) применялась комбинированная спинально-эпидуральная анестезия: в интратекальное пространство вводился наропин 5,0 мл, в эпидуральное пространство - наропин 2 мг/мл в виде постоянной инфузии через перфузор со скоростью 4-6 мл/ч.
Проведение анестезиологического пособия обеспечивала одна и та же бригада врачей для исключения так называемого «человеческого фактора».
Интраоперационный мониторинг показателей проводился согласно Гарвардскому стандарту (электрокардиография, измерение частоты сердечных сокращений (ЧСС), неинвазивное измерение артериального давления (АД), сатурация кислорода (SpO2), капнография, термометрия) в сочетании с биспектральным мониторингом (BIS). У пациентов при общей анестезии поддерживался одинаковый уровень угнетения сознания по BIS < 40–60.
Для выявления синдрома ПОКД всем пациентам была выполнена оценка когнитивных функций при помощи "Монреальской шкалы оценки когнитивных функций (Montreal Cognitive Assessment) – «МОКА-тест»: до оперативного лечения, после операции на 2-4 и на 30 сутки. Также производилась оценка уровня тревожности при помощи теста Спилбергера, концентрации и устойчивости внимания путем пробы Бурдона. Время для проведения тестов составляло не более 15 мин.
Для определения степени риска и частоты возникновения синдрома ПОТР в предоперационном периоде применялась схема, предложенная M.R. Tramer [11] к повседневному использованию в клинической практике. В соответствии с ней, перед оперативным лечением производилась оценка общеклинического (ПОТР в анамнезе, курение), анестезиологического (ингаляционные анестетики, закись азота, опиоиды) и хирургического (вид и продолжительность операции) факторов риска. Антиэметическая профилактика в периоперационном периоде не проводилась.
Результаты и их обсуждение. При обследовании перед оперативным лечением у всех пациентов был выявлен нормальный психоневрологический статус. По результатам МОКА-тест наблюдалось отсутствие каких-либо изменений когнитивной сферы, показатели соответствовали возрастным нормам. На 2-4 сутки после операции у 22 из 50 пациентов (44%, p<0,05) по результатам МОКА-теста наблюдалось снижение когнитивных функций (табл. 1). При этом преимущественно страдали показатели концентрации и устойчивости внимания, а также краткосрочной и долгосрочной памяти. Через 1 месяц после оперативного лечения по результатам МОКА-теста когнитивные нарушения сохранялись у 5 (10%, p<0,05) обследуемых (табл.1). У них отмечалось устойчивое снижение памяти и концентрации внимания.
Таблица 1. Результаты оценки когнитивных функций при помощи МОКА-теста

Примечание: здесь и далее P<0,05.
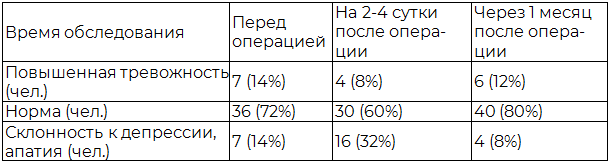
По результатам теста Спилбергера до операции - у 7 из 50 (14%, p<0,05) пациентов отмечалась повышенная тревожность, а еще у 7 из 50 (14%, p<0,05) - склонность к депрессии и апатия (Табл. 2). Уровень тревожности на 2-4 сутки после операции оказался в пределах нормы лишь у 60% (30 из 50, p<0,05). У 4 (8 %, p<0,05) пациентов наблюдалось возбуждение и повышенная тревожность, у 16 (32 %, p<0,05) - угнетение и депрессия (Табл. 2). Также было отмечено, что у 15 обследуемых из 50 (30 %, p<0,05) снижение среднего уровня тревожности и депрессия сопровождались развитием послеоперационных когнитивных дисфункций. Аналогичная картина была выявлена и у 3 пациентов (6%, p=0,05) с повышенной тревожностью. При оценки тревожности спустя 30 дней незначительные изменения различного рода выявлены у 10 пациентов (20 %, p<0,05), при этом когнитивные функции у них были не нарушены (табл. 2).
Таблица 2. Результаты оценки уровня тревожности
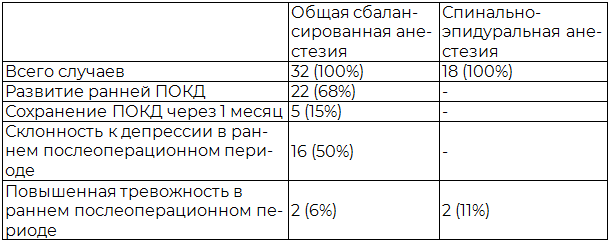
При анализе методов анестезиологического обеспечения у всех пациентов с развившимися ПОКД на 2-4 сутки была выполнена общая сбалансированная анестезия на основе севофлурана и фентанила. В группе со спинально-эпидуральной анестезией случаев развития синдрома ПОКД выявлено не было (табл. 3). Таким образом, частота развития ранней ПОКД при общей сбалансированной анестезии на основе севофлурана и фентанила составила 68% (p<0,05). Также отмечено, что когнитивные нарушения в первой группе через 1 месяц сохранились у 15% пациентов (табл. 3).
При анализе уровня тревожности выявлено, что при применении ОСА на основе севофлурана и фентанила в 50% случаях у больных наблюдалась депрессия и апатия в раннем послеоперационнном периоде. Во второй группе схожих нарушений уровня тревожности отмечено не было. Пациенты с повышенной тревожностью в раннем послеоперационном периоде встречались в первой группе в 6%, а во второй группе в 11% случаях соответственно (табл. 3).
Таблица 3. Зависимость частоты развития ПОКД и изменений тревожности от вида анестезиологического обеспечения
При анализе пробы Бурдона (табл. 4) отмечено, что при применении ОСА на основе севофлурана и фентанила наблюдается снижение показателя концентрации внимания (T) на 2-4 сутки после операции в 31% случаев, через 1 месяц - в 12% (p<0,05). Также в данной группе на всех послеоперационных этапах выявлено снижение темпа выполнения тестовых заданий (А1, А2).
При применении спинально-эпидуральной анестезии снижение показателя концентрации внимания (T) в раннем послеоперационном периоде на 2-4 сутки незначительное - в 8% наблюдений (p<0,05), а через 1 месяц снижение показателей концентрации внимания не зафиксировано (табл.4).
Таблица 4. Результаты теста "проба Бурдона" в зависимости от вида анестезиологического обеспечения
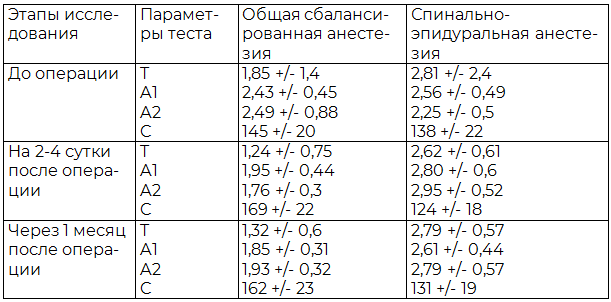
Примечание: T - показатель концентрации внимания, A1 - устойчивость внимания на 1-й минуте, A2 - устойчивость внимания на 2-й минуте, C – время в сек., затраченное на выполнение теста.
При обследованием перед операцией у всех пациентов была выявлена низкая степень риска ПОТР (20-30% по шкале M.R. Tramer). После оперативного лечения в течение первых суток развитие синдрома ПОТР наблюдалось у 40% пациентов (20 из 50, p<0,05). При анализе зависимости анестезиологического обеспечения и частоты ПОТР выявлено, что в первой группе (ОСА на основе севофлурана и фентанила) синдром ПОТР развивался в 53% (17 из 32 случаев, p<0,05), а во второй (спинально-эпидуральная анестезия) - в 16,6% (3 из 18 случаев, p<0,05) (табл. 5).
Таблица 5. Частота развития ПОТР в зависимости от вида анестезиологического обеспечения

Заключение. Таким образом, в 44% случаях после планового оперативного лечения наблюдалось снижение когнитивных функций, что требует назначение специфической профилактики как в послеоперационном периоде, так и интраоперационно. Спустя 30 дней после операции когнитивный дефицит сохраняется у 10% пациентов. Во всех случаях развития синдрома ПОКД использовалась общая сбалансированная анестезия на основе севофлурана и фентанила. Случаев развития синдрома ПОКД при использовании спинально-эпидуральной анестезии зафиксировано не было. Оценка уровня тревожности перед операцией позволяет сделать вывод о недостаточной эффективности и необходимости коррекции премедикации. Отклонение тревожности от среднего уровня в раннем послеоперационном периоде наблюдается в 40%, причем в 100% случаев это сочетается с развитием ПОКД. Частота развития синдрома ПОТР после плановых операций в условиях ОСА на основе севофлурана и фентанила составляет 53% , при спинально-эпидуральной анестезии – 16,6%. Исходя из вышесказанного целесообразно использование регионарных методов анестезии (спинально-эпидуральной анестезии) у больных старческого и пожилого возраста, особенно с плохим состоянием здоровья при выполнении, как тотального протезирования тазобедренного сустава, так и гемиартропластике.
