Существует множество вариантов формирования бедренного туннеля при пластике передней крестообразной связки (ПКС). Наибольшей популярностью пользуются: транстибиальный метод, методы формирования через передне-медиальный порт, методы формирования снаружи-внутрь [3, 12, 14, 19, 22, 23, 25].
Из описанных в литературе недостатков транстибиальной методики можно отметить:
- формирование бедренного канала через большеберцовый туннель, что обуславливает зависимость расположения бедренного туннеля от расположения большеберцового;
- трудности при фиксации винтами вследствие расхождения направления канала и направления фиксации. большой риск повреждения трансплантата при фиксации;
- вертикальное и переднее расположение трансплантата. нарушение кинематики коленного сустава и остаточная нестабильность вследствие слабого контроля «новой связкой» ротации большеберцовой кости;
- более частая необходимость, чем при других методиках, выполнения резекции края межмыщелковой вырезки «notchplasty» при контактном конфликте края межмыщелковой ямки бедренной кости и трансплантата «impingement»;
- увеличение риска возникновения и прогрессирования остеоартроза в сравнении с анатомичными методиками пластики ПКС [6, 8, 13, 20, 21, 24, 27, 28, 30, 31].
Философия анатомической однопучковой реконструкции ПКС предполагает расположение трансплантата относительно центров нативного прикрепления связки на мыщелках бедренной и большеберцовой костей [32].
Для анатомичного расположения бедренного туннеля применяется техника передне-медиального порта. В литературе описаны следующие недостатки данной техники:
- необходимость дополнительного медиального порта, что может привести к ятрогенному повреждению переднего рога медиального мениска, повреждению хряща медиального мыщелка бедренной кости;
- высокий риск повреждения общего малоберцового нерва при проведении направляющей спицы для сверления канала;
- короткий бедренный туннель, что ограничивает возможности прочной фиксации;
- проведение направляющей спицы и рассверливание бедренного туннеля должно производиться при постоянном максимальном сгибании в коленном суставе, что требует дополнительного ассистента хирурга [1, 2, 6, 9, 10, 20, 21, 26, 29, 30].
Учитывая вышеперечисленные недостатки, часть хирургов отдает предпочтение при формировании бедренного туннеля методике снаружи- внутрь. Из недостатков данной методики, описанных в литературе, можно отметить следующие:
- косметический, связанный с формированием дополнительных доступов (центральный через связку надколенника для установки внутрисуставной части направителя, верхне-латеральный для рассверливания туннеля);
- повышенная травматизация трансплантата о край костного туннеля из-за более горизонтального расположения;
- увеличение времени операции [10,11, 27, 28].
Отсутствие в мировой литературе единого мнения о способе формирования бедренного туннеля при реконструкции ПКС говорит о том, что данная тема является весьма актуальной и дискутабельной, обуславливая необходимость данного исследования.
Цели исследования:
- Модификация техники установки бедренного направителя при методике снаружи-внутрь формирования бедренного туннеля при анатомичной реконструкции передней крестообразной связки.
- Послеоперационная оценка расположения бедренного туннеля при помощи КТ и метода квадрантов (Bernard and Hertel) [4].
- Оценка длины бедренного туннеля при данной методике.
Материалы и методы. В данное исследование была включена группа из 15 пациентов с застарелыми повреждениями ПКС, которым в период с 2013 по 2014 г. в ГКБ №12 г. Москвы на базе кафедры травматологии и ортопедии РУДН была выполнена реконструкция ПКС с использованием артроскопической однопучковой «анатомичной» методики с формированием бедренного туннеля при помощи модифицированной техники снаружи-внутрь. Характеристика пациентов: мужчин было 11 (73%), женщин 4 (27%), средний возраст составил 26±8 лет. Повреждений правого коленного сустава было 10 (68%), левого - 5 (32%). Характеристика сочетания повреждений ПКС и менисков показано на рис. 1.
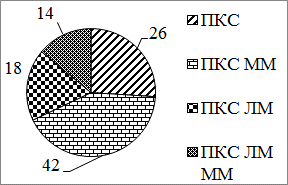
Рис. 1. Характеристика сопутствующих повреждений: ПКС - изолированное повреждение передней крестообразной связки; ПКС ММ - повреждение связки и медиального мениска; ПКС ЛМ - повреждение связки и латерального мениска; ПКС ЛМ ММ - повреждение связки и обоих менисков %.
Оперативная техника. Во всех случаях использовалась спинномозговая (СМА) анестезия с нейровегетативной защитой. Диагностическая артроскопия выполнялась с использованием стандартных передних доступов: передне-латеральный; передне-медиальный-формировался на основании предварительно введенной направляющей инъекционной иглы; также использовался верхне-латеральный доступ для установки промывной канюли. Определялись степень и тип повреждения ПКС, диагностировались сопутствующие внутрисуставные повреждения менисков, хряща и др. В своей работе в качестве пластического материала для замещения поврежденной ПКС мы использовали трансплантат из сухожильных частей полусухожильной и нежной мышц. В качестве имплантов для фиксирования трансплантата использовался биодеградируемый винт в бедре и биодеградируемый винт с гильзой в большеберцовой кости (smith&nephew BIORCI, DePuy BIO-INTRAFIX Tibial Sheath, Tapered Screw). При заборе трансплантата коленному суставу придавалось сгибание 90-95° и выполнялся косой кожный разрез 3-5. Он располагался на 2,5 см медиальнее бугристости большеберцовой кости по направлению к подколенной области в проекции прикрепления сухожилий «гусиной лапки». Далее вдоль волокон вскрывалась сарториальная фасция, выделялись сухожилия полусухожильной и нежной мышц. Преимуществом косого разреза являлась наименьшая вероятность повреждения подкожного нерва. Проксимальную часть фрагментов забирали сухожильным экстрактором с пересечением мышечно-сухожильной части, дистальные концы отсекали вместе с периостом. На препаровочном столике производилась обработка трансплантата. Из полученного материала формировали 4-х пучковый трансплантат в среднем длиной 11 см, диаметром 8 мм. От проксимального конца трансплантата маркером или прошиванием до нужного уровня отмечалось расстояние в 30 мм. Эта метка необходима для определения глубины погружения трансплантата в бедренный костный канал.
Формирование большеберцового туннеля. Наборы механических инструментов позволяли выполнять пластику ПКС, используя метрическую и градусную шкалы. Большеберцовый направитель (Arthrex) имел форму полуокружности и был основан на эффекте перекрещивания двух радиальных осей в одной плоскости в строго определенной точке. Внутрисуставной наконечник большеберцового направителя устанавливался на центр культи ПКС на уровне заднего края переднего рога латерального мениска. На внесуставной дуге направителя заранее выставляли угол, равный 55-60°, по отношению к горизонтальной поверхности плато большеберцовой кости. Направляющая втулка направителя для спицы устанавливалась так, чтобы она проходила через кожный разрез, ранее используемый для забора трансплантата, и упиралась в большеберцовую кость на 1-1,5 см кнутри от медиального края бугристости большеберцовой кости. Маркировочные деления на втулке позволяли определить длину формируемого большеберцового туннеля. По втулке проводили спицу. Далее по спице канюлированной головчатой фрезой или сверлом диаметром равным диаметру трансплантата, в медиальном мыщелке большеберцовой кости формировали сквозной канал «снаружи внутрь».
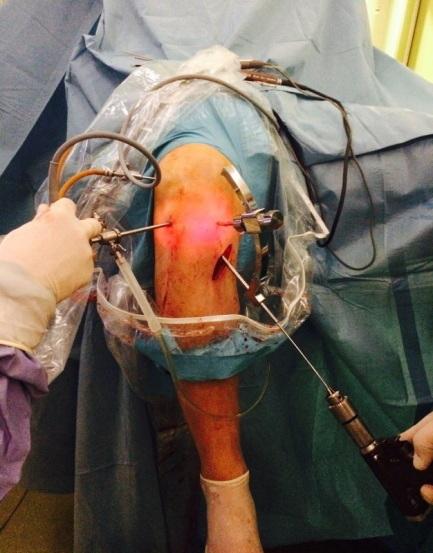
Рис. 2. Формирование большеберцового туннеля.
Формирование бедренного туннеля. Суставу придавалось сгибание 70-90°. При необходимости, выполнялась экономная резекция края межмыщелковой вырезки «notchplasty». Бедренный направитель (Arthrex) имел форму полуокружности и был основан на эффекте перекрещивания двух радиальных осей в одной плоскости в строго определенной точке. При формировании бедренного канала внутрисуставно ориентировались на ниже перечисленные критерии:
- Остатки культи ПКС, в этом случае искомый центр находился в центре культи.
- Латеральный межмыщелковый (Lateral intercondylar ridge) и бифуркационный край (Lateral bifurcate ridge) (Рисунок 3). Для лучшей визуализации данных референтных структур с помощью ручных инструментов, шейвера, радиочастотного электрода удаляли остатки культи ПКС, снимали тонкий слой мягких тканей, покрывающий внутреннюю поверхность наружного мыщелка бедренной кости. Искомый центр смещали на 1,5мм проксимальнее и на 1,5мм кзади от точки пересечения межмыщелкового и бифуркационного края, с учетом того, что область прикрепления передне-внутреннего пучка связки больше, чем задне-наружного.
- В тех случаях, когда после дебридмента не удавалось установить латеральный межмыщелковый и бифуркационный край, с помощью артроскопической линейки производили измерения. Искомый центр бедренного приклепления ПКС находился в 43% от проксимально- дистальной длины латеральной стенки межмыщелковой вырезки и 2,5мм+R (R-радиус трансплантата) от заднего суставного края внутренней поверхности латерального мыщелка бедра [18].
Установленный центр бедренного прикрепления ПКС отмечали при помощи микрофрактора или радиочастотного электрода.
![Рис. 3. Референтные структуры внутренней поверхности наружного мыщелка бедренной кости [7].](/images/articles/2015/4.1/15172/p3.gif)
Рис. 3. Референтные структуры внутренней поверхности наружного мыщелка бедренной кости [7].
![Рис. 4 (A, B). Классическая установка внутрисуставного наконечника бедреннного направителя через центральный порт установленный через связку надколенника [15].](/images/articles/2015/4.1/15172/p4.jpg)
Рис. 4 (A, B). Классическая установка внутрисуставного наконечника бедреннного направителя через центральный порт установленный через связку надколенника [15].
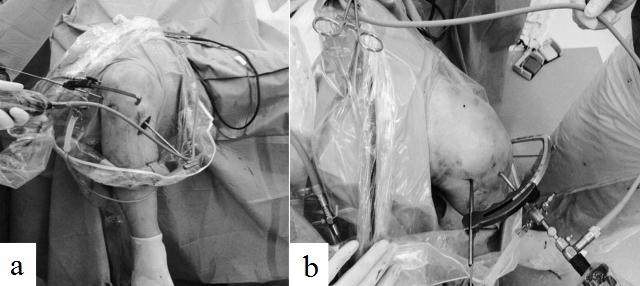
Рис. 5 (a, b). Модифицированная техника установки внутрисуставного наконечника бедренного направителя через стандартный медиальный порт.
По классической методике внутрисуставная часть направителя вводилась через передне-латеральный или через дополнительный центральный порт, установленный через связку надколенника (рис. 4 A, B). При модифицированной технике внутрисуставная часть данного направителя вводилась в сустав через стандартный переднемедиальный порт и устанавливалась на отмеченный участок (рис. 5 a, b). На внесуставной дуге направителя заранее выставляли угол равный 115°. Наклон внесуставной части дуги направителя относительно трансэпикондилярной линии составлял 20-40°, относительно линии перпендикулярной оси бедра - 40-60°. В неё устанавливали направляющую втулку для спицы так, чтобы она проходила через предварительно сформированный кожный разрез длиной 1-1,5 см и упиралась в кость кпереди от латерального надмыщелка бедра. Маркировочные деления на ножке позволяли определить длину формируемого бедренного туннеля. По ножке проводили спицу так, чтобы ее внутрисуставной конец выходил точно в центре расположения предполагаемого бедренного туннеля. На этом этапе для лучшей визуализации места выхода спицы в некоторых случаях производилась временная смена артроскопического доступа с переднелатерального на переднемедиальный. Далее по спице канюлированной головчатой фрезой или сверлом диаметром равным диаметру трансплантата в латеральном мыщелке бедренной кости формировали сквозной канал «снаружи – внутрь». Когда костные каналы оказывались полностью подготовленными, под артроскопическим контролем трансплантат проводился в сустав через большеберцовый костный канал с помощью артроскопического зажима, артроскопического крючка и длинных технологических нитей. Далее спица диаметром 1,1мм вводилась в щель между трансплантатом и краем бедренного костного канала при сгибании коленного сустава от 70° до 90°. При общем натяжении трансплантата по спице вводился интерферентный винт, плотно фиксировавший трансплантат в бедренном канале. Винты обычно использовались диаметром 8 мм и длиною 25 мм, при этом винт вводился до полного погружения головки, максимально в параллельном направлении относительно оси бедренного канала. После фиксации трансплантата в бедренной кости выполнялась оценка изометрии трансплантата. Эти испытания позволяли оценить правильность изометрического расположения трансплантата в костных каналах. Следующий этап операции заключался в фиксировании дистального конца трансплантата в большеберцовом костном канале. Суставу придавалось сгибание 15-30°, трансплантат натягивался до напряжения 8 кг и под артроскопическим контролем фиксировался биорассасывающимся интерферентным винтом с гильзой. До их введения щель между пучками трансплантата последовательно расширялась с помощью расширителей до соответствующего диаметра гильзы. Винты обычно использовались диаметром 7-9 мм и длиною 25-35 мм с максимальным погружением в большеберцовый канал. На последнем этапе артроскопически осматривался созданный аутотрансплантат ПКС, оценивалось его напряжение и взаимоотношение с наружной стенкой мыщелка бедра и «крышей» бедренной вырезки. В исследуемых группах мы не наблюдали контактного конфликта края межмыщелковой ямки бедренной кости и трансплантата «impingement». Сустав промывался; оценивался объём движений, Лахман тест, симптом переднего выдвижного ящика (ПВЯ). В полость сустава на сутки устанавливался активный дренаж. Выполнялось послойное ушивание ран с наложением стерильных повязок. Производилась иммобилизация конечности брейсом.
КТ и метод квадрантов. Всем пациентам в раннем послеоперационном периоде на 5-7 сутки выполнялась компьютерная томография (Toshiba, Aquilion Prime), толщина среза 0,5 мм. Для анализа данных использовалась программное обеспечение (Vital Browser Version 2,2). Выполнялось 3D моделирование, латеральный мыщелок бедра выводился строго в боковую позицию, медиальный мыщелок вырезался. Центр бедренного туннеля определялся при помощи метода квадрантов (Bernard and Hertel), расстояние высчитывалось в процентах от длины ребер прямоугольника вдоль линии Blumensaat в проксимально-дистальном направлении, перпендикулярно линии Blumensaat в передне-заднем направлении [4]. Сравнение полученных результатов производилось с оптимальной позицией, определенной Bird с соавторами [5]. Оптимальным положением считалось расстояние 28% вдоль линии Blumensaat в проксимально-дистальном направлении, 35% перпендикулярно линии Blumensaat передне-заднем направлении (рис. 6).
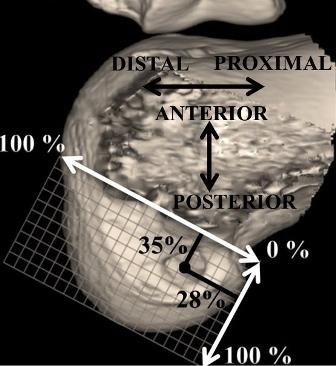
Рис. 6. Центр бедренного туннеля на 3D реконструкции наружного мыщелка бедренной кости: оптимальное положение центра бедренного туннеля.
Результаты и обсуждение. При помощи статистического анализа были вычислены средние значения. В исследуемой группе центр бедренного туннеля был определён на расстоянии 28,2% (от 23% до 35%) вдоль линии Blumensaat в проксимально-дистальном направлении, 35% (от 25% до 45%) перпендикулярно линии Blumensaat в передне-заднем направлении. Длина бедренного туннеля составляла в среднем 34,8 мм (от 28 до 41). Похожие результаты были получены James H. и соавт. 34,1 мм (от 25 до 41,2) [16]. Операционное время составляло 78 мин (от 70 до 90). В 3 (20%) случаях интраоперационно для лучшей визуализации направляющей спицы при формировании бедренного туннеля требовалась смена артроскопического порта с передне-латерального на передне-медиальный, что несколько удлиняло время операции. Ятрогенного повреждения хряща, менисков, общего малоберцового нерва не наблюдалось. Угол наклона внесуставной дуги направителя относительно трансэпикондилярной линии составлял 20-40°, относительно линии перпендикулярной оси бедра- 40-60°. В исследованиях James H. и соавт. было показано, что при формировании бедренного туннеля по методике СВ и установке дуги направителя относительно трансэпикондилярной линии 20° и относительно линии перпендикулярной оси бедра 60° воссоздаваемая длина, ширина, площадь области прикрепления, а также угловая ориентация трансплантата наиболее соответствуют нативной ПКС [17].
Заключение. Установка внутрисуставной части бедренного направителя через стандартный медиальный порт позволяет исключить необходимость максимального сгибания в коленном суставе во время формирования канала в бедренной кости. Также исключается необходимость в дополнительном центральном порте через связку надколенника для внутрисуставной части направителя. Методика «снаружи-внутрь» позволяет установить внутрисуставную часть направителя в нужную позицию без конфликта с мыщелками бедренной кости. Риск ятрогенного повреждения хряща медиального мыщелка бедра и переднего рога медиального мениска снижается, так как отсутствует необходимость выполнения дополнительного медиального порта. Риск повреждения общего малоберцового нерва при использовании методики «снаружи-внутрь» крайне невысок в связи с контролируемым проведением направляющей спицы и рассверливанием бедренного туннеля. Длина бедренного туннеля при данной методике достаточна для плотной фиксации трансплантата. Фиксирующий винт в этом случае вводится по направляющей спице по оси бедренного туннеля. Края внутрисуставной части костного туннеля необходимо сглаживать при помощи головчатой фрезы, что снижает риск повреждения трансплантата.
