Хронический простатит (ХП) занимает ведущее место в структуре урологических заболеваний [1,7], существенно нарушающий качество жизни больных [1,8]. Ряд исследователей [1,4-6] указывают, что у больных ХП одним из звеньев патогенеза заболевания являются нарушения в системе гемостаза, заключающиеся в развитии хронического диссеминированного внутрисосудистого свертывания (ДВС-синдрома) и локальным микротромбозом. Лечение ХП представляет значительные трудности в связи с полисимптомным и полисистемным характером заболевания [2,4-8]. Традиционные методы лечения ХП не обеспечивают необходимого терапевтического эффекта, вызывают ряд побочных и аллергических состояний [5,6]. Поэтому следует изыскивать немедикаментозные методы терапии, к которым относится внутривенное лазерное облучение крови (ВЛОК), обладающее нормализующим влиянием на микроциркуляцию тканей, кислородтранспортную функцию крови [3,4].
Данные литературы о влиянии внутривенного лазерного облучения крови (ВЛОК) на систему гемостаза у больных ХП отсутствуют, что и явилось целью настоящего исследования.
Цель исследования – изучить реологические свойства крови под влиянием ВЛОК у больных ХП.
Материалы и методы исследования. Под нашим наблюдением находилось 60 больных ХП в возрасте от 22 до 45 лет (средний возраст 32,7±1,4 года) с длительностью заболевания от 1 года до 8 лет (в среднем 4,2±1,6 лет).
Клинический диагноз устанавливался на основании субъективных, объективных (ультразвуковое и пальцевое ректальное исследование предстательной железы) и лабораторных (секрет предстательной железы) данных заболевания. Специальными методами исследования исключены заболевания, передающиеся половым путем.
ВЛОК проводили на аппарате «Матрикс-ВЛОК» лазерным излучением в красной области спектра (0,63 мкм) мощностью 1,5-2 мВт на выходе световода одноразовыми стерильными световодами с иглой КИВЛ-01 через день в течение 30 минут, на курс 10 сеансов.
У всех пациентов до и через 30 дней после окончания ВЛОК производили общий клинический анализ крови с определением гемоглобина, гематокрита, числа тромбоцитов, исследование системы гемостаза: определение концентрации фибриногена по Рутберг Р. (г/л); протромбиновый индекс по Квику; общая свертываемость крови оценивалась на тромбоэластографе – определялись величина r+k (мм), отражающая ферментативную фазу свертывания крови, величину mа (мм), характеризующую эластичность сгустка, индекс тромбопластического потенциала (ИТП, усл.ед.). Агрегация тромбоцитов оценивалась фотометрическим методом Borne с использованием в качестве стимуляторов агрегации растворов аденозиндифосфата в концентрации 1 х 10-3 и в реакции коллаген-агрегации. В качестве маркеров внутрисосудистого тромбообразования проводили исследование содержания продуктов деградации фибрина и фибриногена (ПДФ) с помощью теста ингибиции гамагглютинации и полуколичественным методом (латекс-тест) при использовании наборов фирмы «Boehringer Mannheim» (Германия).
Проводилось определение ингибиторов свертывания крови и маркеров фибринолитического звена системы гемостаза: а) активности антитромбина – III (АТ-III) с помощью хромогенных субстратов из набора «Berichrom AT-III Behringwerke» (Германия); б) концентрации АТ-III методом радиальной иммунодиффузии на пластинках «Nor-Partigen» (по Манчини); в) концентрации комплекса тромбин-антитромбин III (Т-АТ-III) с помощью иммуноферментной системы «Ensygnost-ТАТ» на приборе «Vitatron» (Голландия); г) концентрации фибронектина методом радиальной диффузии на пластинах «LC-Partigen» (Германия); д) активности протеина С - ингибитора активированных акселератов свертывания Va и VIIIa с помощью хромогенных субстратов из наборов «Behringwerke» (Германия); е) концентрации кислого альфа-гликопротеида - белка «активной фазы» и ингибитора агрегации тромбоцитов методом радиальной иммунодиффузии на пластинках «Nor-Partigen Behringwerke» (Германия); ж) концентрации плазминогена – основного субстрата фибринолитической системы методом радиальной иммунодиффузии на пластинах «M-Partigen» (по Манчини).
Результаты исследований. У 42% больных содержание фибриногена было повышено (2,9±0,1 г/л) в 1,3 раза по сравнению с нормой (2,3±0,3 г/л, р<0,05). После курса ВЛОК концентрация фибриногена снизилась (р<0,05) до 2,5±0,2 г/л, достигая нормы (р>0,05).
Показатель r+K тромбоэластрограммы у больных был снижен (16,07±0,84 мм) в 1,3 раза по сравнению с нормой (21,43±1,26 мм, р<0,05). После курса ВЛОК показатель r+К достоверно снизился (р<0,05) до 21,24±1,63 мм, соответствуя норме (р>0,05).
Показатель ma у больных был повышен (53,18±1,17 мм) по сравнению с нормой (49,36±1,52 мм, р<0,05). После курса ВЛОК показатель ma достоверно снизился (р<0,05) до 47,56±1,25 мм, достигая нормы (р>0,05).
ИТП у больных был повышен (16,27±1,19 усл. ед.) в 2,3 раза по сравнению с нормой (10,21±1,17 усл.ед., р<0,05). После курса ВЛОК ИТП снизился до 16,29±1,13 усл.ед., достигая нормы (р>0,05).
Содержание тромбоцитов в крови у больных было на верхней границе нормы (348,6±24,7·10 g/л) (норма – 329,4±21,1·10 g/л). Агрегационные свойства тромбоцитов находились на верхней границе нормы как при стимуляции АДФ·10-3 М и соответствовали 43,1±2,7% (норма – 38,7±2,6%), так и при воздействии коллагеном – 50,1±2,3% (норма - 49,4±2,5%). Агрегационная активность тромбоцитов при стимуляции с АДФ·10-3 М после курса ВЛОК составила 38,1±2,4%, достигая нормы. При воздействии коллагеном агрегация тромбоцитов после курса ВЛОК составила 48,9±3,7%, соответствуя норме.
Содержание АТ-III у больных было повышено (0,41±0,01 г/л) в 1,3 раза по сравнению с нормой (0,31±0,02 г/л, р<0,05). После курса ВЛОК концентрация АТ-III составила 0,34±0,03 г/л, достигая нормы (р>0,05), что отражено в табл. 1.
Таблица 1. Показатели звена ингибиторов свертывания крови, фибринолиза и фибринолитического звена системы гемостаза под влиянием внутривенного лазерного облучения крови у больных хроническим простатитом
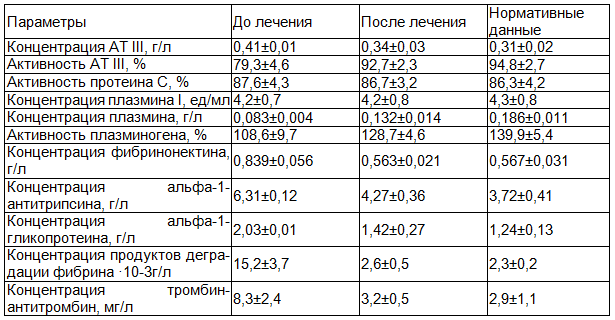
Активность АТ-III у больных была снижена (79,3±4,6%) в 1,2 раза по сравнению с нормой (94,8±2,7%, р<0,05). После курса ВЛОК активность АТIII составила 92,7±2,3%, достигая нормы (р>0,05). Активность протеина С у больных соответствовала норме (87,6±4,3%). Однако, у 32% больных ХП активность протеина С была достоверно (р<0,05) снижена до 70,4±8,3%. Под влиянием ВЛОК активность протеина С у больных существенно не изменилась (р>0,05). Однако, при анализе индивидуальных данных у 32% больных со сниженной активностью протеина С после курса ВЛОК выявлено достоверное (р<0,05) увеличение активности протеина С до 85,3±3,9 % (р<0,05 по сравнению с изначальными данными), достигая нормы (р>0,05%).
Концентрация РА I у больных составила 4,2±0,7 ед/мл, соответствуя норме (4,3±0,8 ед/мл, р>0,05). После курса ВЛОК концентрация РА I существенно не изменилась и составила 4,2±0,8 ед/мл, соответствуя норме (р>0,05).
Концентрация плазминогена у больных была снижена (0,083±0,004 г/л) в 2,2 раза по сравнению с нормой (0,186±0,011 г/л). После курса ВЛОК концентрация плазминогена составляла 0,132±0,014 г/л (р<0,05), не достигая нормы (р<0,05).
Активность плазминогена была снижена (108,6±9,7%) в 1,3 раза по сравнению с нормой (139,9±5,4%, р<0,05). После курса ВЛОК активность плазминогена достоверно (р<0,05) увеличилась до 128,7±4,6% (р<0,05 по сравнению с изначальными данными), не достигая нормы (р<0,05).
Концентрация фибринонектина у больных была повышена (0,839±0,056 г/л) в 1,5 раза по сравнению с нормой (0,567±0,031 г/л, p<0,05). После курса ВЛОК концентрация фибронектина соответствовала 0,563±0,021 г/л (р<0,05), достигая нормы (р>0,05).
Содержание альфа-1-антитрипсина было повышено (6,31±0,12 г/л) в 1,7 раза по сравнению с нормой (3,72±0,41 г/л, р<0,05). После курса ВЛОК концентрация альфа-1-антитрипсина снизилась до 4,27±0,36 г/л (р<0,05), достигая нормы (р>0,05).
Содержание альфа-1-гликопротеина было повышено (2,03±0,01 г/л) в 1,6 раза по сравнению с нормой (1,24±0,13 г/л, р<0,05). После курса ВЛОК концентрация альфа-1-гликопротеина составила 1,42±0,27 г/л (р<0,05), достигая нормы (р>0,05).
У 64% больных концентрация Т-АТ III была повышена (8,3±2,4 мг/л) в 2,9 раза по сравнению с нормой (2,9±1,1 мг/л, р<0,05). После курса ВЛОК концентрация Т-АТ III составила 3,2±0,5 мг/л (р<0,05), достигая нормы (р>0,05).
У больных концентрация ПДФ повышена (15,2±3,7·10-3 г/л) в 6,7 раза по сравнению с нормой (2,3±0,3 ·10-3 г/л). После курса ВЛОК концентрация ПДФ снизилась до 2,6±0,5·10-3 г/л (р<0,05), соответствуя норме (р>0,05).
Количественный анализ показывает, что реологические свойства крови у больных ХП были нарушены у 40 (66,7%), после проведения ВЛОК – у 11 (18,3%), т.е. у 29 (48,4%) больных под влиянием ВЛОК наступила коррекция реологических свойств крови.
Обсуждение. Одним из патогенетических факторов ХП являются нарушения в системе гемостаза, проявляющиеся в развитии гиперкоагуляции на фоне снижения антикоагуляционного потенциала и угнетения фибринолиза, протекающие по типу хронической формы ДВС-синдрома [2,4]. Из немедикаментозных методов лечения при нарушениях гемостаза ВЛОК является адекватным в терапии больных ХП [3,4].
Проведено обследование и лечение ВЛОК 60 больных ХП в возрасте от 22 до 45 лет (средний возраст 32,7±1,4 года).
Показатель r+К тромбоэластограммы у болных был снижен (р<0,05) в 1,3 раза по сравнению с нормой, что свидетельствовало о наличии хронометрической гиперкоагуляции. Показатели ma и ИТП у больных были повышены в 1,08 и 2,3 раза соответственно по сравнению с нормой, что свидетельствовало о высокой степени хронометрической структурной гиперкоагуляции.
После курса ВЛОК показатели r+K, ma и ИТП соответствовали норме (р>0,05), что показывает нормализующее влияние ВЛОК на процесс образования тромбопластина, тромбина и структурные свойства сгустка.
Содержание тромбоцитов, агрегационная активность тромбоцитов как при стимуляции АДФ·10-3 М и коллагеном соответствовали верхним границам нормы, что свидетельствовало о гиперактивности тромбоцитарного звена системы гемостаза у больных ХП. После курса ВЛОК агрегационная активность тромбоцитов при стимуляции АДФ·10-3 М и коллагеном соответствовали норме, что указывает на нормализующее влияние ВЛОК на вязкость крови и тромбоцитарное звено системы гемостаза у больных ХП.
Концентрация АТ-III у больных была повышена (р<0,05), а активность антитромбина – снижена (р<0,05), что свидетельствует о гиперкоагуляции и снижении антикоагулянтного потенциала крови. После ВЛОК концентрация АТ-III и активность антитромбина достигли нормы.
Активность протеина С и концентрация РА у больных соответствовали норме.
Концентрация плазминогена и активность плазминогена у больных были снижены в 2,2 и 1,3 раза соответственно по сравнению с нормой. Известно, что плазминоген является предшественником плазмина, обладающего способностью воздействовать на фибриноген, фибрин, антигемофильный фактор, проакцелерин и фактор Кристмаса, является основным субстратом фибринолитической системы. После курса ВЛОК концентрация плазминогена и активность плазминогена не достигли нормативных данных, однако их концентрации достоверно повысились по сравнению с изначальными данными, что является благоприятным фактором для функционирования фибринолитической системы.
Концентрация фибринонектина (играет роль в адгезии тромбоцитов к коллагену, формировании и угнетении тромбов), альфа-1-антитрипсина, альфа-1-гликопротеина (белков активной фазы, являющихся ингибиторами фибринолиза) были повышены в 1,5, 1,7 и 1,6 раза соответственно по сравнению с нормой, что свидетельствует об угнетении фибринолиза и наличии воспалительного процесса в организме. Фибринонектин синтезируется эндотелием сосудистой стенки, является мультифакториальным фактором системы гемостаза. Кроме того, фибринонектин способен откладываться в местах острого и хронического воспаления, приводящего к быстрому развитию фиброзирующих и склеротических процессов в пораженных тканях. На фоне обнаруженных изменений в системе гемостаза в организме больных активизируются аутоиммунные процессы, что поддерживает течение ХП. После курса ВЛОК их концентрации достигли нормы, что является благоприятным прогностическим фактором для улучшения процессов фибринолиза, о чем свидетельствуют также результаты, полученные другими исследователями [4].
У больных концентрация Т-АТ-III (наиболее информативный и ранний тест для диагностики внутрисосудистого свертывания крови) и ПДФ были повышены в 2,9 и 6,7 раза по сравнению с нормой, что свидетельствует о хронической тромбинемиии и хронической компенсированной форме ДВС-синдрома. В связи с активацией тромбиногенеза в организме АТ III связывается с тромбином и превращается в неактивный комплекс Т-АТ-III. После курса ВЛОК концентрации Т-АТ-III и ПДФ соответствовали норме, что свидетельствует о купировании тромбонемии и ДВС-синдрома.
Заключение. В результате ВЛОК реологические свойства крови нормализовались у 44 (73,3%) из 40 больных, у которых ранее были нарушены реологические свойства крови. После проведения ВЛОК происходит стабилизация коагуляционного потенциала крови за счет плазменного и тромбоцитарного звеньев гемостаза и усиления активности ингибиторов свертывания и повышения фибринолитического потенциала крови, снижение процессов внутрисосудистого свертывания. Коагуло- и реокорригирующий эффект ВЛОК связан, очевидно, с элиминацией микробных эндо- и экзотоксинов, вазоактивных веществ, играющих роль в нарушении микроциркуляции и внутрисосудистой агрегации тромбоцитов. Наши результаты согласуются с данными других исследователей, которые указывают на корригирующий эффект ВЛОК на систему гемостаза у больных с различными терапевтическими и хирургическими заболеваниями, сопровождающимися развитием ДВС-синдрома [3,4].
